题目内容
25℃时,下图烧杯中各盛有25mL的溶液.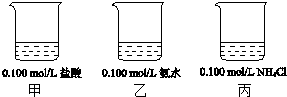
(1)甲溶液pH=
(2)若将甲溶液全部倒入乙中,所得的混合溶液的pH(填“>”、“<”或“=”)
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,所得溶液中离子浓度大小顺序是
分析:(1)pH=-lgc(H+);
(2)等体积等物质的量浓度的盐酸和氨水恰好反应生成氯化铵,氯化铵是强酸弱碱盐,其溶液呈酸性,浓度不同的氯化铵溶液,浓度越小,其溶液的PH越大;
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,说明一水合氨是电离程度大于铵根离子的水解程度,根据溶液的酸碱性结合电荷守恒确定离子浓度大小.
(2)等体积等物质的量浓度的盐酸和氨水恰好反应生成氯化铵,氯化铵是强酸弱碱盐,其溶液呈酸性,浓度不同的氯化铵溶液,浓度越小,其溶液的PH越大;
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,说明一水合氨是电离程度大于铵根离子的水解程度,根据溶液的酸碱性结合电荷守恒确定离子浓度大小.
解答:解:(1)氯化氢是强电解质,在水中完全电离,所以c(H+)=c(HCl)=0.100mol/L,所以pH=-lgc(H+)=-lg0.100=1,故答案为:1;
(2)等体积等物质的量浓度的盐酸和氨水恰好反应生成氯化铵,氯化铵是强酸弱碱盐,其溶液呈酸性,溶液混合时体积增大一倍,浓度是丙中的一半,氯化铵的浓度越小,其酸性越弱,所以混合溶液的pH大于丙,
故答案为:>;
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,说明一水合氨是电离程度大于铵根离子的水解程度,所以得c(OH-)>c(H+),溶液中存在电荷守恒,c(NH4+)+c(H+)=c(Cl-)+c(OH-),所以得c(NH4+)>c(Cl-),则溶液中离子浓度大小顺序是c(NH4+)>c(Cl-)>c(OH-)>c(H+),
故答案为:c(NH4+)>c(Cl-)>c(OH-)>c(H+).
(2)等体积等物质的量浓度的盐酸和氨水恰好反应生成氯化铵,氯化铵是强酸弱碱盐,其溶液呈酸性,溶液混合时体积增大一倍,浓度是丙中的一半,氯化铵的浓度越小,其酸性越弱,所以混合溶液的pH大于丙,
故答案为:>;
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,说明一水合氨是电离程度大于铵根离子的水解程度,所以得c(OH-)>c(H+),溶液中存在电荷守恒,c(NH4+)+c(H+)=c(Cl-)+c(OH-),所以得c(NH4+)>c(Cl-),则溶液中离子浓度大小顺序是c(NH4+)>c(Cl-)>c(OH-)>c(H+),
故答案为:c(NH4+)>c(Cl-)>c(OH-)>c(H+).
点评:本题考查了pH的简单计算、离子浓度大小的比较等知识点,根据pH的计算公式及电荷守恒来分析即可,难度不大.

练习册系列答案
相关题目







 2NH3(g);
2NH3(g);
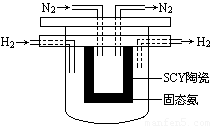
 2NH3(g);△H=-92.4 kJ/mol,他因此获得了1918年度诺贝尔化学奖。试回答下列问题:
2NH3(g);△H=-92.4 kJ/mol,他因此获得了1918年度诺贝尔化学奖。试回答下列问题:



