题目内容
为了除去KCl中的Ca2+,Mg2+,SO42-及泥沙,得到纯净的KCl,可将固体溶于水,然后在下列操作中选取必要的步骤和最佳的操作顺序( )
①过滤 ②加过量KOH溶液 ③加适量盐酸 ④加过量K2CO3溶液 ⑤加过量BaCl2溶液.
①过滤 ②加过量KOH溶液 ③加适量盐酸 ④加过量K2CO3溶液 ⑤加过量BaCl2溶液.
| A、②①⑤①④①③ |
| B、④①②⑤③ |
| C、②⑤④①③ |
| D、①④②⑤③ |
考点:化学实验操作的先后顺序
专题:化学实验基本操作
分析:为了除去粗KCl中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的KCl,先过滤除去泥沙,再加KOH除去Mg2+,加过量BaCl2溶液除去SO42-,加过量K2CO3溶液除去Ca2+及过量钡离子,最后加适量盐酸,以此来解答.
解答:
解:为了除去KCl中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的KCl,先过滤除去泥沙,再加KOH除去Mg2+,加过量BaCl2溶液除去SO42-,加过量K2CO3溶液除去Ca2+及过量钡离子,过滤除去沉淀,最后加适量盐酸,则正确的顺序为②⑤④①③.
故选:C.
故选:C.
点评:本题以KCl提纯考查混合物分离提纯实验方案的设计,为高频考点,明确除杂质的顺序是解答本题的关键,注意碳酸钾一定在氯化钡之后为解答的易错点,题目难度不大.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
下列装置中电流表指针会发生偏转的是( )
A、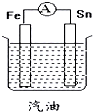 |
B、 |
C、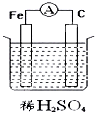 |
D、 |
 某研究性学习小组用如图所示装置研究不同能量之间的转化问题.下列说法正确的是( )
某研究性学习小组用如图所示装置研究不同能量之间的转化问题.下列说法正确的是( )| A、断开开关S1,按下开关S2,此时构成的装置属于电解池 |
| B、断开开关S1,按下开关S2,化学能转化为电能,电能转化为光能等 |
| C、断开开关S2,按下开关S1,此时构成的装置属于原电池 |
| D、断开开关S2,按下开关S1,化学能转化为电能 |
下列说法中不正确是( )
| A、为保护地下钢管不受腐蚀,可使它与直流电源正极相连 |
| B、生铁比纯铁易生锈 |
| C、钢铁发生电化腐蚀比化学更普遍 |
| D、钢铁发生电化腐蚀时其负极反应为;Fe-2e-═Fe2+ |
 如图是一定条件下N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )
如图是一定条件下N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92kJ?mol-1 |
| B、a曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热不变 |
| D、在相同温度的条件下,在体积相同I、II两个容器中分别通入1mol N2和3 mol H2,容器I体积恒定,容器II体积可变保持恒压,则反应过程中两容器内的反应速率v(I)<v(II) |
将100ml、0.1mol/L的BaCl2溶液中加入到100ml、0.2mol/L的H2SO4溶液中,则溶液中存在的离子浓度的关系的是( )
| A、[H+]>[Cl-]>[Ba2+]>[SO42-] |
| B、[Cl-]>[H+]>[SO42-]>[Ba2+] |
| C、[H+]>[Cl-]>[SO42-]>[Ba2+] |
| D、[Cl-]>[H+]>[Ba2+]>[SO42-] |
可逆反应N2+3H2?2NH3(各物质均为气体)的正、逆反应速率可用单位时间内各反应物或生成物浓度的变化来表示.下列各关系中能说明该反应已达到平衡状态的是( )
| A、3v正(N2)=v正(H2) |
| B、v正(N2)=v逆(NH3) |
| C、2 v正(H2)=3 v逆(NH3) |
| D、2v逆(NH3)=3 v正(H2) |
下列关于焓变的叙述中正确的是( )
| A、化学反应的焓变与反应的方向性无关 |
| B、化学反应的焓变直接决定了反应的方向 |
| C、焓变为正的反应都是吸热反应 |
| D、焓变为负的反应都能自发进行 |
下列物质中存在自由移动的氯离子( )
| A、KCl固体 |
| B、熔融KClO3 |
| C、HCl气体 |
| D、NaCl溶液 |