题目内容
火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也激励着我们去刻苦学习、奋发图强.黑火药在发生爆炸时的反应是:2KNO3+C+S═K2S+2NO2↑+CO2↑.其中被还原的元素是 ,K2S中硫离子的结构示意图是 ,氧化剂是 ,还原剂是 ,若爆炸时反应共转移了2mol的电子,则总共能产生 升的气体.
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应2KNO3+C+S═K2S+2NO2↑+CO2↑中,N和S元素化合价降低,被还原,则KNO3和硫为氧化剂,C元素化合价升高,被氧化,C为还原剂,结合化合价的变化解答该题.
解答:
解:反应2KNO3+C+S═K2S+2NO2↑+CO2↑中,N和S元素化合价降低,被还原,则KNO3和硫为氧化剂,还原产物为K2S和NO2,C元素化合价升高,被氧化,C为还原剂,反应中只有C以上化合价升高,化合价由0价升高到+4价,若爆炸时反应共转移了2mol的电子,则生成0.5molCO2,1molNO2,共1.5mol,体积为33.6L,K2S中硫离子的结构示意图是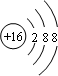 ,
,
故答案为:N、S; ;KNO3和硫;C;33.6L.
;KNO3和硫;C;33.6L.
 ,
,故答案为:N、S;
 ;KNO3和硫;C;33.6L.
;KNO3和硫;C;33.6L.
点评:本题考查氧化还原反应知识,侧重于基本概念的理解,注意从元素化合价的角度分析相关概念并判断物质具有的性质,难度不大.

练习册系列答案
相关题目
Na2O2、CaC2都是离子化合物,都能与水反应放出气体.它们 ( )
| A、阴阳离子个数比均为1:1 |
| B、都含有非极性的共价键 |
| C、与水都发生氧化还原反应 |
| D、放出的都是可燃性气体 |
下列物质放在空气中,不会发生变质的物质是( )
| A、Na |
| B、NaCl |
| C、NaOH |
| D、Na2O2 |
在2A+B=3C+4D的反应中,下列表示该反应速率最大的是( )
| A、VA=0.5mol/(L.min) |
| B、VB=0.3mol/(L.min) |
| C、Vc=2.4mol/(L.min) |
| D、VD=1mol/(L.min) |
下列哪一个反应表示二氧化硫被还原( )
| A、SO2+2H2O+Cl2=H2SO4+2HCl |
| B、SO2+2NaOH=Na2SO3+H2O |
| C、SO2+2H2S=2H2O+3S↓ |
| D、SO2+PbO2=PbSO4 |
下列离子方程式正确的是( )
| A、NaAlO2溶液中通入少量二氧化碳:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、碳酸镁和盐酸混合:CO32-+2H+=CO2↑+H2O |
| C、NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O=Fe(OH)2↓+2HClO |
| D、碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑ |