题目内容
11.某同学组装了如图所示的原电池装置,下列叙述中正确的是( )
| A. | 电子方向:Zn→Cu | |
| B. | Cu电极逐渐溶解 | |
| C. | Zn电极上发生还原反应 | |
| D. | 盐桥中装有含氯化钾的琼脂,Cl-向右池移动 |
分析 A、电子由负极锌经导线流向正极铜;
B、铜极上是铜离子放电生成单质铜;
C、负极发生氧化反应;
D、阴离子向负极移动.
解答 解:A、电子由负极锌经导线流向正极铜,所以电子方向:Zn→Cu,故A正确;
B、铜极上是铜离子放电生成单质铜,锌溶解而非铜溶解,故B错误;
C、负极发生氧化反应,所以Zn电极上发生氧化反应,故C错误;
D、阴离子向负极移动,所以氯离子向左池移动,故D错误;
故选A.
点评 本题考查了原电池原理,明确正负极上得失电子、盐桥中阴阳离子移动方向、电子和电流的流向即可解答,难度不大.

练习册系列答案
相关题目
2.下列关于NH4+、NH3、NH2-三种微粒的说法不正确的是( )
| A. | 三种微粒所含有的电子数相等 | B. | 三种微粒中氮原子的杂化方式相同 | ||
| C. | 三种微粒的空间构型相同 | D. | 键角大小关系:NH4+>NH3>NH2- |
19.NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| B. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后得到NH3分子数为NA | |
| C. | 1.0L的0.1 mol•L-1Na2S溶液中含有的S2-离子数为0.1NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
6.链型的不饱和油酸(C17H33COOH)与蔗糖反应可以制得非天然油脂,其反应示意图如图所示(图中的反应式不完整),则下列说法不正确的是( )
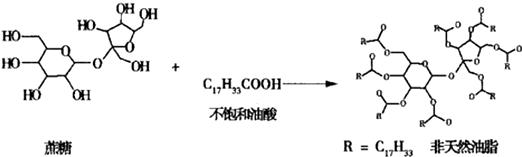

| A. | 该非天然油脂与氢氧化钠溶液共热,产物可与溴的四氯化碳溶液反应 | |
| B. | 天然油脂、蔗糖、非天然油脂都能发生水解反应 | |
| C. | 蔗糖、葡萄糖分别与银氨溶液水浴加热反应,有相同的实验现象 | |
| D. | 植物油、非天然油脂都可以与H2发生加成反应 |
16.图为烃分子的球棍模型,“大球”表示碳原子,“小球”表示氢原子.下列说法正确的是( )
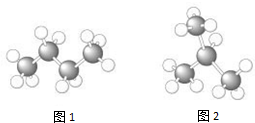

| A. | 图1表示的烃叫丙烷 | |
| B. | 图2烃分子的结构简式为CH3CH2CH2CH3 | |
| C. | 图1与图2表示的是同一种物质 | |
| D. | 图1与图2表示的物质互为同分异构体 |
20.已知元素R的某种同位素形成的离子化合物的化学式为AmRn,该晶体中一个R粒子的核外电子是a,核内中子数是b,则该同位素的原子符号是( )
| A. | ${\;}_{a}^{b}$R | B. | ${\;}_{a}^{a+b}$R | C. | ${\;}_{a-m}^{a+b-m}$R | D. | ${\;}_{a+m}^{a+b+m}$R |
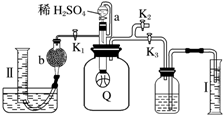 为了测定已部分变质的过氧化钠样品的纯度,设计如图所示的实验装置,图中Q为弹性良好的气球(不与药品反应),称取一定量的样品放入其中.按如图所示的装置安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球中.
为了测定已部分变质的过氧化钠样品的纯度,设计如图所示的实验装置,图中Q为弹性良好的气球(不与药品反应),称取一定量的样品放入其中.按如图所示的装置安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球中.