题目内容
(14分)为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
【探究一】
(1)常温下,工业上用铁质容器盛放冷的浓硫酸,其原因是 。
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用 (选填序号)。a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此可求算气体Y中SO2的体积分数。
写出探究②中出现的所有离子反应方程式 。
【探究二】
根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893g·L-1。为此设计了下列探究实验装置(图中夹持仪器省略,假设有关气体完全反应)。
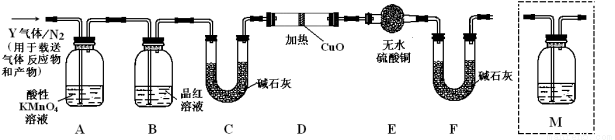
(3)装置B中试剂的作用是 。
(4)分析Y气体中的Q2气体是如何生成的 。(用化学方程式表示)。
(5)为确认Q2的存在,需在装置中添加洗气瓶M于 (选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是 。
(1)铁表面被钝化,阻止了内部金属与酸的进一步反应(2分);(2)①d(2分);
②SO2+Cl2+2 H2O=SO42-+2Cl-+4H+ SO42- +Ba 2+= BaSO4↓(2分);
(3)检验SO2是否除尽(2分);(4)C+2H2SO4(浓) CO2↑+2SO2↑+2 H2O(2分);
CO2↑+2SO2↑+2 H2O(2分);
(5)C(2分); (6)D中的固体由黑变红和E中固体由白变蓝(2分)
【解析】
试题分析:(1)常温下,铁遇冷的浓硫酸发生氧化还原反应,在铁表面生成一层致密的氧化物薄膜而阻止了进一步的反应,即发生钝化现象,所以常温下,工业上用铁质容器盛放冷的浓硫酸;
(2)①亚铁离子具有还原性,而酸性高锰酸钾有氧化性,发生氧化还原反应使高锰酸钾溶液褪色,故答案为:d;
②SO2具有还原性,能使溴水褪色,反应的离子方程式为SO2+Cl2+2 H2O=SO42-+2Cl-+4H+,生成硫酸与氯化钡反应生成硫酸钡白色沉淀,离子方程式为SO42- +Ba 2+= BaSO4↓;
(3)二氧化硫能使品红溶液褪色,所以用品红溶液检验二氧化硫是否除尽;
(4)碳素钢中含有碳,加热条件下,碳能和浓硫酸反应生成二氧化硫、二氧化碳和水,反应方程式为C+2H2SO4(浓) CO2↑+2SO2↑+2 H2O;
CO2↑+2SO2↑+2 H2O;
(5)二氧化硫和二氧化碳都能使澄清石灰水变浑浊,但二氧化硫还能使品红溶液褪色,所以要检验二氧化碳必须排除二氧化硫的干扰,B装置是检验二氧化硫是否除尽,所以澄清石灰水应放置在B和C之间,即在通入碱石灰之前检验,故答案为:C;
(6)Q1气体,在标准状况下,密度为0.0893g?L-1,其相对分子质量为2,所以是氢气,氢气具有还原性,能还原黑色的氧化铜生成红色的铜单质,同时生成水,水能使无水硫酸铜变蓝色,这是检验水的特征反应,所以如果D中氧化铜变红,E中无水硫酸铜变蓝,则证明含有氢气。
考点:考查浓硫酸的性质、二氧化硫的性质、常见物质的检验等

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案下列离子或物质组能大量共存,且满足相应条件的是
选项 | 离子或物质 | 条件 |
A | Na+、K+、Cl-、SO42- | c(Na+)+c(K+)=c(SO42-)+ c(Cl-) |
B | Fe3+ 、SO32-、Cl- | 加入NaOH溶液,产生红褐色沉淀 |
C | Ba+ 、HCO3-、Cl-、H+ | 加入氨水产生沉淀 |
D | SO2、O2、NO2 | 通入足量NaOH溶液后,可能会没有任何气体剩余 |
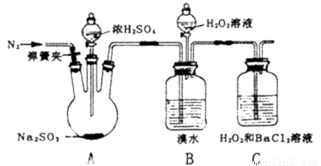
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
实验操作 | 实验现象 |
i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化,继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)A中发生反应的化学方程式是 .
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2.
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是 .
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是 .
③iii中滴入少量H2O2没有明显变化.提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是 .
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是 .
 NH3·2H2O + HCl
NH3·2H2O + HCl