题目内容
13.四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,该反应的氧化剂是KNO3、S,当1mol C参与反应时转移4mol电子,请用双线桥描述S+2KNO3+3C=K2S+N2↑+3CO2↑电子转移情况 .
.
分析 该反应中,硫元素化合价由0价变为-2价,N元素化合价由+5价变为0价,碳元素化合价由0价变为+4价,根据元素化合价变化判断氧化剂和还原剂,氧化剂在反应中被还原,还原剂在反应中被氧化,以此解答.
解答 解:反应S+2KNO3+3C═K2S+N2↑+3CO2↑中,S元素化合价由0价降低到-2价,则S为氧化剂,N元素化合价由+5价降低到0价,则KNO3为氧化剂,C元素化合价由0价升高到+4价,则C为还原剂,还原剂对应的氧化产物为CO2,氧化剂对应的还原产物为K2S、N2,反应中1molC失去4mol电子,该反应中转移电子数为4e-,则转移的电子方向和数目为 .;
.;
故答案为:S、KNO3;4; .
.
点评 本题考查氧化还原反应,侧重于学生的分析能力的考查,明确元素的化合价的变化及氧化还原反应中的基本概念是解答本题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.在一定温度下的定容容器中,不能表明反应A(s)+2B(g)?C(g)+D(g)已达到平衡状态的( )
| A. | 混合气体的密度不变 | B. | 混合气体的压强不变 | ||
| C. | 混合气体的平均相对分子质量不变 | D. | 的转化率不变 |
4.HM和HR的溶液分别加水稀释时pH变化如图.下列叙述中正确的是( )
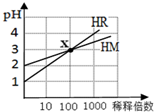

| A. | HR可能是弱酸 | B. | x点时c(R-)=c(M-) | ||
| C. | HM是一种强酸 | D. | 稀释前,c(HR)=10c(HM) |
18.对于下列反应的反应类型的判断,正确的是( )
| A. | CO2+H2O=H2CO3分解反应 | |
| B. | Cu(OH)2$\frac{\underline{\;△\;}}{\;}$CuO+H2O 化合反应 | |
| C. | Fe2O3+3CO$\frac{\underline{\;△\;}}{\;}$2Fe+3CO2 置换反应 | |
| D. | NaCl+AgNO3=AgCl↓+NaNO3复分解反应 |
2.部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.92g,如附图所示流程处理,下列说法中,正确的是( )
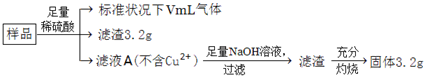
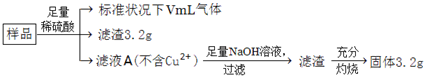
| A. | 滤液A中阳离子不可能含H+、Fe2+、Fe3+ | |
| B. | 样品中金属Fe的质量为2.24g | |
| C. | 样品中CuO的质量为4.0g | |
| D. | V=224 |