题目内容
磷在氧气中燃烧,可能生成两种固态氧化物。(1)通过计算确定反应产物的组成(用化学式表示)是 ,其相应的质量(g)为 。
(2)已知单质磷的燃烧热为Y kJ·mol-1,则1 mol P与O2反应生成固态P2O3的反应热ΔH= 。
(3)写出1 mol P与O2反应生成固态P2O3的热化学方程式: 。
解析:(1)P在O2中燃烧可能生成P2O3和P2O5,据题意判断,O2不足,产物为P2O3和P2O5的混合物。
设有x mol P生成P2O3,y mol P生成P2O5,则有:

解得![]()
则生成P2O3 0.025 mol,生成P2O5 0.025 mol。
m(P2O3)=0.025 mol×110 g·mol-1=2.75 g
m(P2O5)=0.025 mol×142 g·mol-1=3.55 g
(2)据题意,3.1 g磷燃烧生成0.025 mol P2O3、0.025 mol P2O5,共放热X kJ,则生成0.025 mol P2O3共放热(X-0.025Y)kJ,故1 mol P与O2反应生成0.5 mol P2O3放出的热量为(20X-Y) kJ,即ΔH=-(20X-Y)kJ·mol-1
答案:(1)P2O3、P2O5 2.75、3.55
(2)-(20X-Y)kJ · mol-1
(3)P(s)+![]() O2(g)
O2(g) ![]()
![]() P2O3(s);
P2O3(s);
ΔH=-(20X-Y)kJ·mol-1

练习册系列答案
相关题目
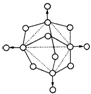 磷在空气中充分燃烧,生成X的分子结构如右图所示.图中实线表示化学键,圆圈表示原子(不考虑原子体积大小)
磷在空气中充分燃烧,生成X的分子结构如右图所示.图中实线表示化学键,圆圈表示原子(不考虑原子体积大小)