题目内容
甲、乙两烧瓶中各盛有100mL3mol·L-1的盐酸和氢氧化钾溶液;向两烧瓶中分别加入等质量的铝粉,反应结束测得生成的气体体积甲∶乙=2∶3(相同状况),则加入铝粉的质量为
A.2.7g B.3.6g C.5.04g D.4.05g
D
【解析】
试题分析:Al与盐酸、NaOH反应的方程式是:2Al+6HCl=2AlCl3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑。若Al足量,等物质的量的电解质反应产生的氢气的物质的量的比是1:3,现在产生的氢气的物质的量的比是2:3,说明Al对酸足量,对碱来说不足量,n(HCl)=0.3mol,则与酸反应产生的氢气的物质的量是0.3mol÷2=0.15mol;由于向两烧瓶中分别加入等质量的铝粉,反应结束测得生成的气体体积甲∶乙=2∶3,所以Al与碱反应产生的氢气的物质的量是n(H2)=3/2×0.15mol=0.225mol,根据方程式中Al与氢气的物质的量关系可知:n(Al)=2/3×0.225mol=0.15mol.所以m(Al)= 0.15mol×27g/mol=4.05g.因此选项是D。
考点:考查Al与等量的酸、碱发生反应产生氢气的物质的量的关系的知识。

(13分)根据要求完成下列各小题实验目的。(a、b 为弹簧夹,加热及固定装置已略去)
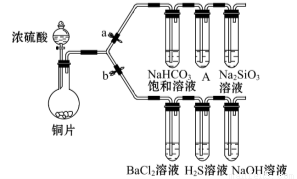
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸 >碳酸)
①连接仪器、 、加药品后,打开a关闭 b,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是__________________,装置A中的试剂是 。
③能说明碳的非金属性比硅强的实验现象是:_______________________。
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性。
①打开b,关闭a。能验证SO2具有氧化性的化学方程式是:___________。
②若大量的SO2通入NaOH溶液中,其化学方程式是:__________________。
③BaCl2溶液中无沉淀现象,将其分成两份,分別滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氯 水 | 氨 水 |
沉淀的化学式 |
|
|
写出其中SO2 显示还原性并生成沉淀的离子方程式___________________。

 、Al3+ 和X四种离子以物质的量之比2:4:1:1大量共存于同一溶液中,则X可能是 A.Cl– B.Na+ C.OH– D.
、Al3+ 和X四种离子以物质的量之比2:4:1:1大量共存于同一溶液中,则X可能是 A.Cl– B.Na+ C.OH– D. 