题目内容
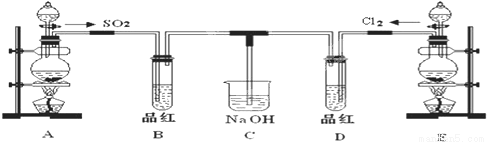
(13分)根据要求完成下列各小题实验目的。(a、b 为弹簧夹,加热及固定装置已略去)
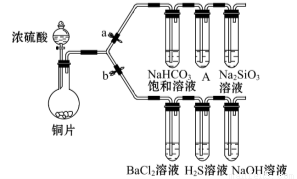
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸 >碳酸)
①连接仪器、 、加药品后,打开a关闭 b,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是__________________,装置A中的试剂是 。
③能说明碳的非金属性比硅强的实验现象是:_______________________。
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性。
①打开b,关闭a。能验证SO2具有氧化性的化学方程式是:___________。
②若大量的SO2通入NaOH溶液中,其化学方程式是:__________________。
③BaCl2溶液中无沉淀现象,将其分成两份,分別滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
滴加的溶液 | 氯 水 | 氨 水 |
沉淀的化学式 |
|
|
写出其中SO2 显示还原性并生成沉淀的离子方程式___________________。
(13分) (1) ①检验装置的气密性(1分)
②Cu+2H2SO4(浓) 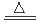 CuSO4+SO2↑+2H2O(1分)酸性KMnO4溶液(1分)
CuSO4+SO2↑+2H2O(1分)酸性KMnO4溶液(1分)
③A中酸性KMnO4溶液不褪色,Na2SiO3溶液中出现白色沉淀(2分)
(2) ①2H2S+SO2==3S↓+2H2O(2分)②SO2+NaOH ==NaHSO3(2分)
③(各1分)BaSO4 、BaSO3。Ba2++SO2+Cl2+2H2O==BaSO4↓+4H++2Cl-(2分)
【解析】
试题分析:①连接仪器、检验装置的气密性、加药品后,打开a关闭 b,然后滴入浓硫酸,加热。这时发生反应产生SO2气体。②铜与浓硫酸反应的化学方程式是Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O;由于SO2溶于水产生H2SO3,由于酸性H2SO3> H2CO3,所以在饱和NaHCO3溶液中发生反应,NaHCO3+ SO2= CO2+ NaHSO3,微粒证明C、Si的非金属性强弱,所以应该把混在产生CO2气体的SO2气体装置A中除去,该装置的试剂是酸性KMnO4溶液;若A中紫色变浅,证明SO2气体被除去干净,CO2气体通入到Na2SiO3,会发生反应:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓,形成白色沉淀;故③能说明碳的非金属性比硅强的实验现象是:A中酸性KMnO4溶液不褪色(或变浅),Na2SiO3溶液中出现白色沉淀;(2) ①打开b,关闭a。能验证SO2具有氧化性的实验现象是H2S溶液中产生淡黄色沉淀,反应的化学方程式是2H2S+SO2=3S↓+2H2O;②若大量的SO2通入NaOH溶液中,会发生反应形成酸式盐,其化学方程式是SO2+NaOH =NaHSO3;③由于酸性HCl> H2SO3,所以向BaCl2溶液中通入SO2,只是产生少量的H2SO3,而无沉淀现象,当向其中加入氯水时,会发生反应:Cl2+SO2+2H2O=H2SO4+2HCl。H2SO4+BaCl2=BaSO4↓+2HCl,产生BaSO4白色沉淀;若向其中加入氨水,则会发生反应:SO2+2NH3·H2O=(NH4)2SO3+H2O, (NH4)2SO3+BaCl2=BaSO3↓+2NH4Cl,产生BaSO3白色沉淀。其中SO2 显示还原性并生成沉淀的离子方程式是Ba2++SO2+Cl2+2H2O==BaSO4↓+4H++2Cl-。
CuSO4+SO2↑+2H2O;由于SO2溶于水产生H2SO3,由于酸性H2SO3> H2CO3,所以在饱和NaHCO3溶液中发生反应,NaHCO3+ SO2= CO2+ NaHSO3,微粒证明C、Si的非金属性强弱,所以应该把混在产生CO2气体的SO2气体装置A中除去,该装置的试剂是酸性KMnO4溶液;若A中紫色变浅,证明SO2气体被除去干净,CO2气体通入到Na2SiO3,会发生反应:Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓,形成白色沉淀;故③能说明碳的非金属性比硅强的实验现象是:A中酸性KMnO4溶液不褪色(或变浅),Na2SiO3溶液中出现白色沉淀;(2) ①打开b,关闭a。能验证SO2具有氧化性的实验现象是H2S溶液中产生淡黄色沉淀,反应的化学方程式是2H2S+SO2=3S↓+2H2O;②若大量的SO2通入NaOH溶液中,会发生反应形成酸式盐,其化学方程式是SO2+NaOH =NaHSO3;③由于酸性HCl> H2SO3,所以向BaCl2溶液中通入SO2,只是产生少量的H2SO3,而无沉淀现象,当向其中加入氯水时,会发生反应:Cl2+SO2+2H2O=H2SO4+2HCl。H2SO4+BaCl2=BaSO4↓+2HCl,产生BaSO4白色沉淀;若向其中加入氨水,则会发生反应:SO2+2NH3·H2O=(NH4)2SO3+H2O, (NH4)2SO3+BaCl2=BaSO3↓+2NH4Cl,产生BaSO3白色沉淀。其中SO2 显示还原性并生成沉淀的离子方程式是Ba2++SO2+Cl2+2H2O==BaSO4↓+4H++2Cl-。
考点:考查碳、硅非金属性的相对强弱的比较及SO2的氧化性、还原性、酸性的检验方法的知识。

 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
 MnCl2+Cl2↑+2H2O。若有0.6 mol的HCl参加反应,则转移的电子总数为 mol;
MnCl2+Cl2↑+2H2O。若有0.6 mol的HCl参加反应,则转移的电子总数为 mol;