题目内容
8.对于AgCl(s)?Ag++Cl-,平衡后欲使溶液中的[Cl-]增大,可采取的措施是①③⑤⑥①加氨水 ②加水 ③加NaCl(s) ④加AgCl(s) ⑤加NaBr(s) ⑥加热.
分析 对于AgCl(s)?Ag++Cl-,平衡后欲使溶液中的[Cl-]增大,可加入可溶性氯化物,或加入与Ag+反应的物质,使平衡正向移动,另外加热促进溶解,以此解答该题.
解答 解:①加氨水,与Ag+发生络合反应生成银氨络离子,平衡正向移动,可氯离子浓度增大,故正确;
②加水,如仍为饱和溶液,则离子浓度不变,如为不饱和溶液,则浓度减小,故错误;
③加NaCl(s),可使氯离子浓度增大,故正确;
④加AgCl(s),平衡不移动,氯离子浓度不变,故错误;
⑤加NaBr(s),生成AgBr沉淀,平衡正向移动,氯离子浓度增大,故正确;
⑥加热,促进溶解,氯离子浓度增大,故正确.
故答案为:①③⑤⑥.
点评 本题考查难溶电解质的溶解平衡,为高频考点,侧重考查学生的分析能力,注意把握影响平衡移动的因素,难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
9.一定量的铁粉与足量2mol/L盐酸反应,为了加快反应速率且不影响产生氢气的量,可向溶液中加入( )
①3mol/L的硝酸溶液
②少量CuSO4(s)
③加入一定量的铜
④少量CH3COONa(s)
⑤对溶液加热(假定盐酸溶质不挥发)
⑥向反应液中通入HCl气体
⑦加入过量铁粉
⑧加入NaHSO4固体.
①3mol/L的硝酸溶液
②少量CuSO4(s)
③加入一定量的铜
④少量CH3COONa(s)
⑤对溶液加热(假定盐酸溶质不挥发)
⑥向反应液中通入HCl气体
⑦加入过量铁粉
⑧加入NaHSO4固体.
| A. | ②③④⑤⑥ | B. | ③⑤⑥ | C. | ①③⑤⑥⑦ | D. | ③⑤⑥⑧ |
19. 实验室制备环己酮的反应原理:
实验室制备环己酮的反应原理: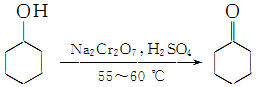 (实验装置如图所示,环己醇、环己酮、饱和食盐水和水的部分物理性质见表).
(实验装置如图所示,环己醇、环己酮、饱和食盐水和水的部分物理性质见表).
(1)实验中通过装置B将酸性Na2Cr2O7溶液加到盛有环己醇的A中,在55~60℃进行反应.反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物.
①仪器A的名称是三颈烧瓶
②仪器A中的反应温度应控制在55~60℃,控制温度的方法是55~60℃水浴加热
③蒸馏不能分离环己酮和水的原因是环已酮和水形成具有固定组成的恒沸物一起蒸出
(2)环己酮的提纯需要经过以下一系列的操作:
a.在收集到的粗品中加NaCl固体至饱和,静置,分液
b.加入无水MgSO4固体
c.抽滤
d.蒸馏,收集151~156℃馏分,得到精品
①在反应装置图中牛角管上的支管的作用是与大气连通,保持内外压强一致
②加入无水MgSO4固体的作用是去除有机物中水分
③抽滤需要使用的仪器为抽气泵、吸气瓶、布氏漏斗.
 实验室制备环己酮的反应原理:
实验室制备环己酮的反应原理: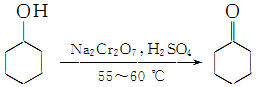 (实验装置如图所示,环己醇、环己酮、饱和食盐水和水的部分物理性质见表).
(实验装置如图所示,环己醇、环己酮、饱和食盐水和水的部分物理性质见表).| 物质 | 沸点(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1 | 0.962 | 能溶于水 |
| 环己酮 | 155.6 | 0.948 | 微溶于水 |
| 饱和食盐水 | 108.0 | 1.330 | - |
| 水 | 100.0 | 0.998 | - |
①仪器A的名称是三颈烧瓶
②仪器A中的反应温度应控制在55~60℃,控制温度的方法是55~60℃水浴加热
③蒸馏不能分离环己酮和水的原因是环已酮和水形成具有固定组成的恒沸物一起蒸出
(2)环己酮的提纯需要经过以下一系列的操作:
a.在收集到的粗品中加NaCl固体至饱和,静置,分液
b.加入无水MgSO4固体
c.抽滤
d.蒸馏,收集151~156℃馏分,得到精品
①在反应装置图中牛角管上的支管的作用是与大气连通,保持内外压强一致
②加入无水MgSO4固体的作用是去除有机物中水分
③抽滤需要使用的仪器为抽气泵、吸气瓶、布氏漏斗.
16.下面各组物质的类别全部正确的是( )
| A | 盐酸:强电解质 | Cl2:非电解质 | CaCO3:弱电解质 |
| B | CuSO4•5H2O:纯净物 | Al(OH)3:一元酸 | HD:单质 |
| C | Al2O3:离子化合物 | NaHCO3:正盐 | Na2O2:碱性氧化物 |
| D | 血液:胶体 | NO2:酸性氧化物 | H2O和D2O:混合物 |
| A. | A | B. | B | C. | C | D. | D |
20.某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )

| A. | 甲装置:可用来证明碳酸的酸性比硅酸强 | |
| B. | 乙装置:橡皮管的作用是能使水顺利流下 | |
| C. | 丙装置:用图示的方法不能检查此装置的气密性 | |
| D. | 丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气 |
17.25℃、l0lkPa下,煤炭、氢气、天然气和甲醇(CH3OH)四种燃料的热值(指一定条件不,单位质量的物质完全燃烧生成稳定氧化物所放出的热量)依次是33kJ•g-1、143kJ•g-1、56kJ•g-1、23kJ•g-1.则下列热化学方程式正确的是( )
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-396 kJ•mol-1 | |
| B. | 2H2(g)+O2(g)=2H2O (l)△H=-286 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)=CO2(g)+2H2O (g)△H=-896 kJ•mol-1 | |
| D. | CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-736 kJ•mol-1 |
18.如图为氢氧燃料电池的工作原理示意图.下列叙述正确的是( )


| A. | b电极是负极 | |
| B. | 供电时的总反应为:2H2+O2═2H2O | |
| C. | 工作时溶液中阴离子移向正极 | |
| D. | 工作时正极区pH升高,负极区pH降低 |

 .(铋元素与氮元素同主族)
.(铋元素与氮元素同主族) 如图所示,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-(配离子)物质的量浓度的对数.
如图所示,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-(配离子)物质的量浓度的对数.