题目内容
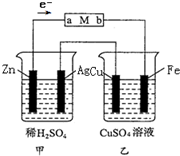 以下装置是某活动小组进行实验的装置图,回答下列问题.
以下装置是某活动小组进行实验的装置图,回答下列问题.(1)甲装置是
(2)M是用紫色石蕊试液浸润过的试纸,则试纸的a端出现的现象是
(3)乙装置中Fe极的电极反应式为
为
考点:原电池和电解池的工作原理
专题:
分析:(1)多池相连含最活泼金属的电极是原电池,其它是电解池,由此分析解答;
(2)a与电源负极相连是电解池的阴极,氢离子放电生成氢气,破坏水的电离平衡,使得氢氧根离子浓度大于氢离子浓度,所以紫色石蕊试液变蓝色;
(3)Fe极是阴极电解质溶液中的铜离子放电,生成单质铜,生成1mol铜转移2mol电子.
(2)a与电源负极相连是电解池的阴极,氢离子放电生成氢气,破坏水的电离平衡,使得氢氧根离子浓度大于氢离子浓度,所以紫色石蕊试液变蓝色;
(3)Fe极是阴极电解质溶液中的铜离子放电,生成单质铜,生成1mol铜转移2mol电子.
解答:
解:(1)最活泼的是锌所以甲池是原电池;Ag极上是氢离子放电,生成氢气,现象是有气泡产生;Zn极的是负极发生氧化反应,电极反应式为:Zn-2e-=Zn2+,故答案为:原电池;有气泡产生;Zn-2e-=Zn2+;
(2)a与电源负极相连是电解池的阴极,氢离子放电生成氢气,破坏水的电离平衡,使得氢氧根离子浓度大于氢离子浓度,所以紫色石蕊试液变蓝色,故答案为:a端试纸变蓝色;水电离出来的H+在a端获得电子发生反应,使该端OH-浓度增大;
(3)Fe极是阴极电解质溶液中的铜离子放电,生成单质铜,电极反应式为:Cu2++2e-=Cu,Fe极增重0.64g,即生成0.01mol铜转移0.02mol电子,故答案为:Cu2++2e-=Cu;0.02mol.
(2)a与电源负极相连是电解池的阴极,氢离子放电生成氢气,破坏水的电离平衡,使得氢氧根离子浓度大于氢离子浓度,所以紫色石蕊试液变蓝色,故答案为:a端试纸变蓝色;水电离出来的H+在a端获得电子发生反应,使该端OH-浓度增大;
(3)Fe极是阴极电解质溶液中的铜离子放电,生成单质铜,电极反应式为:Cu2++2e-=Cu,Fe极增重0.64g,即生成0.01mol铜转移0.02mol电子,故答案为:Cu2++2e-=Cu;0.02mol.
点评:本题考查原电池和电解池原理,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握原电池和电解池的工作原理,把握电极方程式的书写,难度不大.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
下列叙述正确的是( )
| A、1 mol CO2 的质量为44g/mol |
| B、H2SO4的摩尔质量为98 |
| C、标准状况下,气体摩尔体积约为22.4 L |
| D、O2的相对分子质量为32 |
X、Y、Z、W、Q是五种短周期元素,它们在周期表中的位置如图.下列说法不正确的是( )
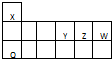

| A、Z与W可形成的化合物在5种以上 |
| B、Z、W、Q三种元素形成的化合物,其水溶液一定呈中性 |
| C、X、Y、Z、W形成的化合物的化学式可以是Y2X7W2Z |
| D、X与Y、Z、W均可形成原子个数比为2:1的化合物 |
对于反应2CO(g)+O2(g)?2CO2(g)(△H<0),在一定条件下建立化学平衡后,下列各条件变化时,能使平衡向正方向移动的是( )
| A、恒容通入少量He |
| B、恒容通入少量CO2 |
| C、升高温度 |
| D、缩小容器体积 |
下列物质转化无法实现的是( )
A、Al2O3
| |||||
B、S
| |||||
C、Fe2O3
| |||||
D、MgCl2(aq)
|
电化学降解NO3-的原理如图所示.下列说法正确的是( )
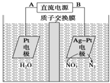

| A、电源正极为B |
| B、阳极反应式为2NO3-+6H2O+10e-=N2↑+12OH- |
| C、当产生N211.2L时,电路中通过的电子数为5NA |
| D、若电解过程中转移了2 mol电子,则两极产生的气体的质量差为10.4g |
当可逆反应2SO2(g)+O2(g)═2SO3(g)达到平衡后,向平衡体系中充入一定量的18O2气体,当反应再次达到平衡时,18O原子( )
| A、只存在于O2中 |
| B、只存于SO3中 |
| C、同时存在于O2和SO3中 |
| D、同时存在于O2、SO2和SO3中 |
对有机物 的化学性质叙述错误的是( )
的化学性质叙述错误的是( )
 的化学性质叙述错误的是( )
的化学性质叙述错误的是( )| A、加热时能被新制的银氨溶液氧化 |
| B、能使酸性KMnO4溶液褪色 |
| C、能发生加聚反应 |
| D、1 mol该物质只能与l molH2加成 |