题目内容
17.下列叙述中,不正确的是( )| A. | 无论在纯水中,还是在稀溶液中,由水电离出的c(H+)与c(OH-)相等 | |
| B. | pH=7的溶液不一定呈中性,c(H+)=c(OH-) 的溶液才是中性溶液 | |
| C. | 无论是酸溶液还是碱溶液中,由水电离出的c(H+)小于纯水电离出的c(H+) | |
| D. | 常温下,在1 mol/L 盐酸中,水的离子积Kw>1×10-14 |
分析 A.结合水的电离方程式H2O?H++OH-分析;
B.溶液酸碱性与溶液中氢离子、氢氧根离子浓度有关,不能直接根据溶液pH判断;
C.酸溶液和碱溶液都抑制了水的电离;
D.水的离子积与温度有关,温度不变,则水的离子积不变.
解答 解:A.根据H2O?H++OH-可知,无论在纯水中,还是在稀溶液中,由水电离出的c(H+)与c(OH-)相等,故A正确;
B.温度影响水的电离,则pH=7的溶液不一定呈中性;溶液酸碱性与溶液中氢离子、氢氧根离子浓度有关,当c(H+)=c(OH-) 时溶液一定呈中性,故B正确;
C.酸溶液中的氢离子、碱溶液中的氢氧根离子都抑制了水的电离,则由水电离出的c(H+)小于纯水电离出的c(H+),故C正确;
D.常温下,在1 mol/L 盐酸中水的离子积不变,则该溶液中水的离子积Kw=1×10-14,故D错误;
故选D.
点评 本题考查弱电解质的电离及其影响、溶液酸碱性判断等知识,题目难度不大,明确溶液酸碱性的判断方法为解答关键,注意水的离子积与温度有关,与溶液酸碱性无关,为易错点.

练习册系列答案
相关题目
2.常温下,下列说法正确的是( )
| A. | 将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 | |
| B. | pH=8.3的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 将0.1 mol/LNaOH溶液与0.06 mol/L硫酸溶液等体积混合,混合溶液的PH=2.0 | |
| D. | Na2CO3溶液中加水稀释后恢复至原温度,pH和Kw均减小 |
8.下列离子方程式不正确的是( )
| A. | 碳酸氢钙溶液跟硝酸反应:Ca(HCO3)2+2H+=Ca2+++2H2O+2CO2↑ | |
| B. | 碘化钾溶液跟适量溴水反应:2I-+Br2=I2+2Br- | |
| C. | 将金属钠加入水中:2Na+2H2O=2Na++2OH-+H2↑ | |
| D. | 将氯气通人氯化亚铁溶液中2Fe2++C12=2Fe3++2Cl- |
5.下列叙述错误的是( )
| A. | 1mol任何物质都含有6.02×1023个原子 | |
| B. | 0.012kg12C 含有阿伏加德罗常数个碳原子 | |
| C. | 在使用摩尔表示物质的量的单位时,应指明粒子的种类 | |
| D. | 物质的量是国际单位制中七个基本物理量之一 |
12.下列关于金属的叙述正确的是( )
| A. | 金属元素在自然界中都是以化合态存在于海水,矿物中 | |
| B. | 通常情况下,金属具有导电性、导热性、和延展性 | |
| C. | 金属活动性顺序表中排在氢前的金属都能与酸反应置换出酸中的氢 | |
| D. | 合金的硬度,熔点一般比组成金属高 |
2.仪器名称为“容量瓶”的是( )
| A. | 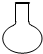 | B. |  | C. | 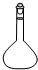 | D. |  |
9.由NO与NO2组成的混合气体中氮元素的质量分数为$\frac{35}{91}$,则混合气体中NO与NO2的体积比为( )
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 35:56 |
6.含下列某种杂质的氯化钠样品,经测定氯的质量分数为62.0%,则该样品中含有的杂质可能是( )
| A. | MgCl2 | B. | ZnCl2 | C. | BaCl2 | D. | KCl |
7.卤素互化物的化学性质跟卤素单质相似,其氧化性介于形成该互化物两卤素单质之间.溴化碘(IBr)是卤素互化物的一种,这种化合物在常温常压下是深红色的固体,熔点为41℃,沸点为116℃.下列对IBr的叙述中,错误的是( )
| A. | 溴化碘能与金属和非金属反应 | B. | 它可与水反应:IBr+H2O→HBrO+HI | ||
| C. | 它可KI溶液反应 KI+IBr→KBr+I2 | D. | 固体溴化碘是一种分子晶体 |