题目内容
20.完成下列问题(1)64g氧气含有2mol氧分子,4mol氧原子;
(2)58.5gNaCl中含Na+的个数约为6.02×1023.
分析 (1)依据m=nM结合氧气为双原子分子解答;
(2)58.5NaCl的物质的量n(NaCl)=$\frac{m}{M}$=$\frac{58.5g}{58.5g/mol}$=1mol,所含有 Na+的个数约为6.02×1023;
解答 解:(1)氧气摩尔质量为32g/mol,则64g氧气含有氧气分子的物质的量为:$\frac{64g}{32g/mol}$=2mol,含有氧原子物质的量为2mol×2=4mol;
故答案为:2mol;4mol;
(2)58.5NaCl的物质的量n(NaCl)=$\frac{m}{M}$=$\frac{58.5g}{58.5g/mol}$=1mol,所含有 Na+的个数约为6.02×1023,故答案为:6.02×1023.
点评 本题考查了物质的量的相关计算,明确摩尔质量概念及计算公式,熟悉氧气为双原子分子是解题关键,题目难度不大.

练习册系列答案
相关题目
11.A、B、C、D为四种短周期元素,已知A、C同主族,B、D同周期;A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层.下列叙述正确的是( )
| A. | 原子序数:A>B>C>D | B. | 单质熔点:D>B,A>C | ||
| C. | 原子半径:C>B>D>A | D. | 简单离子半径:C>A>D>B |
12.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 电解精炼铜时,阴极质量增加6.4g,电路中电子转移的总数为0.2NA | |
| B. | 6.0gSiO2晶体中含有0.2NA个Si-O键 | |
| C. | 10g 46%乙醇溶液中含氧原子0.1NA | |
| D. | 苯与液溴反应生成1mol 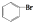 时消耗0.5NA个Br2 时消耗0.5NA个Br2 |
10.化学与生产、生活、环境密切相关.下列说法错误的是( )
| A. | 用食醋清洗热水瓶中的水垢 | |
| B. | 红宝石、珍珠、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 | |
| C. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化物有关 | |
| D. | 绿色化学的核心是利用化学原理从源头上减少或消除工业生产对环境的污染 |