题目内容
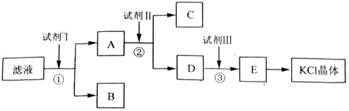
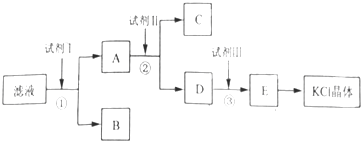
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质.为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,在将滤液按图所示步骤进行操作.回答下列问题:
(1)起始滤液的pH
(2)试剂Ⅰ的化学式为
(3)③中发生反应的化学方程式为

(1)起始滤液的pH
大于
大于
7(填“大于”、“小于”或“等于”),其原因是(用方程式表达)碳酸根离子水解呈碱性
碳酸根离子水解呈碱性
(2)试剂Ⅰ的化学式为
BaCl2
BaCl2
,(3)③中发生反应的化学方程式为
K2CO3+2HCl═CO2↑+H2O+KCl
K2CO3+2HCl═CO2↑+H2O+KCl
.分析:氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质,除去碳酸根离子和硫酸根离子,需要加入过量氯化钡溶液;然后过滤后获得碳酸钾、氯化钾溶液A,然后加入过量的碳酸钾溶液除去溶液中的氯化钡,过滤,得到氯化钾和碳酸钾混合液,再加入过量盐酸,除去过量的碳酸钾,最后通过加入浓缩、蒸发结晶和氯化钾,
(1)根据碳酸钾溶液中碳酸根离子水解进行分析;
(2)根据要除掉杂质离子硫酸根离子和碳酸根离子选择试剂;
(3)根据要除掉多余的碳酸根离子不能引进新的杂质选择试剂,并且写出反应化学方程式.
(1)根据碳酸钾溶液中碳酸根离子水解进行分析;
(2)根据要除掉杂质离子硫酸根离子和碳酸根离子选择试剂;
(3)根据要除掉多余的碳酸根离子不能引进新的杂质选择试剂,并且写出反应化学方程式.
解答:解:氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质,除去碳酸根离子和硫酸根离子,需要加入过量氯化钡溶液;然后过滤后获得碳酸钾、氯化钾溶液A,然后加入过量的碳酸钾溶液除去溶液中的氯化钡,过滤,得到氯化钾和碳酸钾混合液,再加入过量盐酸,除去过量的碳酸钾,最后通过加入浓缩、蒸发结晶和氯化钾
(1)碳酸钾是强碱弱酸盐能水解导致溶液中氢氧根离子浓度大于氢离子浓度,所以溶液呈碱性,pH>7,
故答案为:大于;碳酸根离子水解呈碱性;
(2)要除掉杂质离子硫酸根离子和碳酸根离子,应加入过量的氯化钡溶液,碳酸根和硫酸根生成不溶于水的钡盐,同时生成氯化钾,
故答案为:BaCl2;
(3)要除掉多余的碳酸根离子,要滴加适量的盐酸,碳酸根离子和盐酸反应生成二氧化碳和水,化学方程式为K2CO3+2HCl═CO2↑+H2O+KCl,
故答案为:K2CO3+2HCl═CO2↑+H2O+KCl.
(1)碳酸钾是强碱弱酸盐能水解导致溶液中氢氧根离子浓度大于氢离子浓度,所以溶液呈碱性,pH>7,
故答案为:大于;碳酸根离子水解呈碱性;
(2)要除掉杂质离子硫酸根离子和碳酸根离子,应加入过量的氯化钡溶液,碳酸根和硫酸根生成不溶于水的钡盐,同时生成氯化钾,
故答案为:BaCl2;
(3)要除掉多余的碳酸根离子,要滴加适量的盐酸,碳酸根离子和盐酸反应生成二氧化碳和水,化学方程式为K2CO3+2HCl═CO2↑+H2O+KCl,
故答案为:K2CO3+2HCl═CO2↑+H2O+KCl.
点评:本题考查了氯化钾的提纯,注意在解此类题时,首先分析需要除去的杂质的离子,选择试剂时,既要除杂彻底,还不能引入新的杂质,硫酸根离子一般放在开始除去,碳酸根离子将剩余的钡离子除去,最后加盐酸除剩余的碳酸根离子,本题难度中等.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目