��Ŀ����
 ��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��
��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��
 CO2��g��+3H2��g�� CH3OH��g��
CO2��g��+3H2��g�� CH3OH��g��
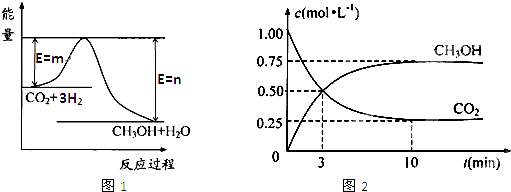
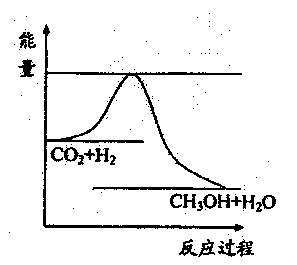
+H2O��g������ͼ��ʾ�÷�Ӧ���й���
�������ı仯��
��1���÷�Ӧ�ġ�H 0
����>��<��=����
��2���÷�Ӧƽ�ⳣ��K�ı���ʽΪ
��
��3���¶Ƚ��ͣ�ƽ�ⳣ��K ����
�������������䡱��С������
��4��Ϊ̽����Ӧԭ�����ֽ�������ʵ�飺
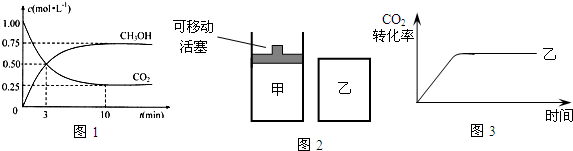
�����Ϊ1 L���ܱ������У�����
1mol CO2 ��3molH2�����CO2��
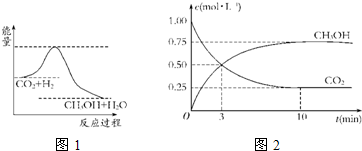
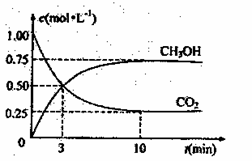 CH3OH��g����Ũ����ʱ�ʱ仯����ͼ��ʾ��
CH3OH��g����Ũ����ʱ�ʱ仯����ͼ��ʾ��
�ٴӷ�Ӧ��ʼ��ƽ�⣬������Ũ�ȱ仯��
ʾ��ƽ����Ӧ����v��H2��=
�����д�������ʹn��CH3OH��/
n��CO2��������� u��
A�������¶�
B���������
C����H20��g������ϵ�з���
D���ٳ���l molC02��3 mol H2
E������He��g����ʹ��ϵ��ѹǿ����
��5���״���O2��KOH��Һ�ɹ���ȼ�ϵ�أ��为����ӦʽΪ
��12�֣�ÿ��2�֣�
��1��<
��2��c��CH3OH����c��H2O����c��CO2����c��H2��3
��3������
��4����0��225mol����L��min����C��D
��5��CH3OH-6e-+8OH+=CO32-+6H2O

 ������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2��g��+3H2��g��
������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2��g��+3H2��g�� CH3OH��g��+H2O��g����������ͼ��ʾ�÷�Ӧ���й�������������λΪkJ?mol-1���ı仯��
CH3OH��g��+H2O��g����������ͼ��ʾ�÷�Ӧ���й�������������λΪkJ?mol-1���ı仯��