题目内容
18.下列反应必须加入还原剂才能实现的是( )| A. | CO32-→CO2 | B. | Na→Na2O | C. | KMnO4→MnO2 | D. | SO2→S |
分析 必须加入还原剂才能实现,说明给予物质作氧化剂,在反应中得电子化合价降低,据此分析解答.
解答 解:A.该反应中各元素化合价不变,不需要发生氧化还原反应就能实现,故A错误;
B.Na元素化合价由0价变为+1价,所以Na是还原剂,需要氧化剂才能实现,如氧气,故B错误;
C.该反应中Mn元素化合价由+7价变为+6价,则高锰酸钾是氧化剂,但不需要加入还原剂也能实现,如直接加热,故C错误;
D.该反应中S元素化合价由+4价变为0价,则二氧化硫是氧化剂,需要还原剂才能实现,如硫化氢等,故D正确;
故选D.
点评 本题以氧化剂、还原剂判断为载体考查氧化还原反应,明确元素化合价变化与氧化剂、还原剂关系是解本题关键,易错选项是C.

练习册系列答案
相关题目
8.一种直接肼燃料电池的结构如图所示,下列说法正确的是( )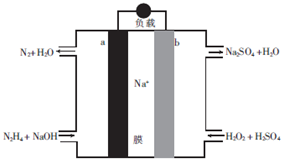

| A. | a极为电池的正极 | |
| B. | 电路中每转移6.02×1023个电子,则有1molNa+穿过膜向正极移动 | |
| C. | b极的电极反应式为H2O2+2e-=2OH- | |
| D. | 用该电池电解饱和食盐水,当阳极生成2.24L(标准状况)Cl2时,消耗肼0.1mol |
6.根据下表所示化学反应与数据关系:
请回答:
(1)反应①是吸热(填“吸热”或“放热”)反应.
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=$\frac{{K}_{2}}{{K}_{1}}$(用K1、K2表示).
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有CE(填写字母序号).
A、缩小反应容器的容积 B、扩大反应容器的容积 C、升高温度
D、使用合适的催化剂 E、设法减小平衡体系中的CO的浓度
(4)若反应③的逆反应速率与时间的关系如图所示:
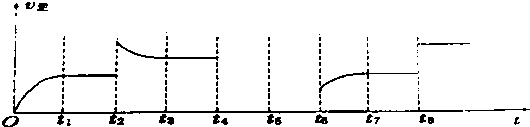
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时增大生成物浓度或升高温度,t8时加入催化剂或加压.
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g) | K3 | ? | ? |
(1)反应①是吸热(填“吸热”或“放热”)反应.
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=$\frac{{K}_{2}}{{K}_{1}}$(用K1、K2表示).
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有CE(填写字母序号).
A、缩小反应容器的容积 B、扩大反应容器的容积 C、升高温度
D、使用合适的催化剂 E、设法减小平衡体系中的CO的浓度
(4)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时增大生成物浓度或升高温度,t8时加入催化剂或加压.
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
13.世界气候变化哥本哈根会议讨论了导致全球气候变暖的主要物质是下列中的( )
| A. | N2 | B. | O2 | C. | CO2 | D. | SO2 |
10.在1000℃时,可逆反应:Fe(s)+CO2(g)?FeO(s)+CO(g)的平衡常数K=2.如果在充有一定量CO2的恒容密闭容器中加入足量的Fe,在1000℃时使之发生上述反应,达平衡时CO2的转化率为( )
| A. | 10% | B. | 33.3% | C. | 50% | D. | 66.7% |
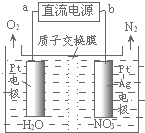 发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.
发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注. 已知A、B、D、E均为中学化学常见物质,它们之间的转化关系如图所示(部分产物略去,①②③④的反应条件均相同).则A、E可能的组合为( )
已知A、B、D、E均为中学化学常见物质,它们之间的转化关系如图所示(部分产物略去,①②③④的反应条件均相同).则A、E可能的组合为( )
