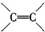
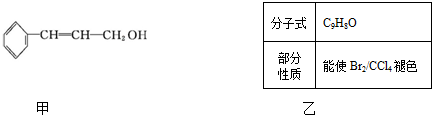
题目内容
写出下列各烷烃的分子式.
(1)烷烃A在同温同压下蒸气的密度是H2的43倍 .
(2)1L烷烃C的蒸气完全燃烧时,生成同温同压下15L的水蒸气 .
(3)分子中含有22个共价键的烷烃D为 .
(1)烷烃A在同温同压下蒸气的密度是H2的43倍
(2)1L烷烃C的蒸气完全燃烧时,生成同温同压下15L的水蒸气
(3)分子中含有22个共价键的烷烃D为
考点:有机物实验式和分子式的确定
专题:有机物分子组成通式的应用规律
分析:(1)根据密度之比等于摩尔质量之比进行计算;
(2)根据同温同压下,体积比等于物质的量之比,再根据氢原子守恒计算出n;
(3)烷烃的组成为CnH2n+2,含有的共价键数目为3n+1,据此分析.
(2)根据同温同压下,体积比等于物质的量之比,再根据氢原子守恒计算出n;
(3)烷烃的组成为CnH2n+2,含有的共价键数目为3n+1,据此分析.
解答:
解:烷烃的通式为:CnH(2n+2),烷烃的相对分子量为:14n+2,
(1)密度之比等于摩尔质量之比,就等于相对分子质量之比,A的相对分子质量为:14n+2=43×2,解得n=6,即该烷烃的分子式为C6H14,
故答案为:C6H14;
(2)1L烷烃D的蒸气完全燃烧时,生成同温、同压下15L水蒸气,根据氢原子守恒,所以烷烃C分子中含30个氢原子,即2n+2=30,n=14,所以C的分子式为C14H30,
故答案为:C14H30;
(3)烷烃的组成为CnH2n+2,含有的共价键数目为3n+1,该烷烃有22个共价键,则:3n+1=22,解得n=7,所以该烷烃中碳原子数目为7,分子式为C7H16.
故答案为:C7H16.
(1)密度之比等于摩尔质量之比,就等于相对分子质量之比,A的相对分子质量为:14n+2=43×2,解得n=6,即该烷烃的分子式为C6H14,
故答案为:C6H14;
(2)1L烷烃D的蒸气完全燃烧时,生成同温、同压下15L水蒸气,根据氢原子守恒,所以烷烃C分子中含30个氢原子,即2n+2=30,n=14,所以C的分子式为C14H30,
故答案为:C14H30;
(3)烷烃的组成为CnH2n+2,含有的共价键数目为3n+1,该烷烃有22个共价键,则:3n+1=22,解得n=7,所以该烷烃中碳原子数目为7,分子式为C7H16.
故答案为:C7H16.
点评:本题考查了有机物烷烃分子式的确定,题目难度中等,要求学生掌握物质的量与摩尔质量转化关系、同温同压下气体的摩尔质量与密度关系.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
下列对KHSO4的物质类型进行的分析,其中不正确的是( )
| A、根据元素组成知它是化合物 |
| B、因为含有钾元素与硫酸根,故KHSO4是钾盐 |
| C、KHSO4可以称为酸式盐 |
| D、因为它含有与酸相同的元素氢,故KHSO4也可称为酸 |
下列离子方程式正确的是( )
| A、碳酸钙与盐酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| B、锌与盐酸反应:Zn+2H++2Cl-═Zn2++2Cl-+H2↑ |
| C、氯化铁与氢氧化钡溶液反应:2Fe3++3Ba(OH)2═2Fe(OH)3↓+3Ba2+ |
| D、氢氧化铜与硫酸反应:OH-+H+═H2O |
下列叙述中正确的是( )
| A、VSEPR模型就是分子的空间构型 |
| B、在共价化合物分子中一定存在σ键 |
| C、全由非金属元素组成的化合物一定是共价化合物 |
| D、共价键键长越短,键能一定越大 |
某化学反应2X(g)?Y(g)+Z(g)在4种不同条件下进行,Y、Z起始浓度为0,反应物X的浓度(mol?L-1)随反应时间(min)的变化情况如下表:
下列说法不正确的是( )
| 实验 序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A、C>1.0 |
| B、实验2可能使用了催化剂 |
| C、实验3比实验2先达到化学平衡状态 |
| D、前10分钟,实验4的平均化学反应速率比实验1的大 |
化学与科学、技术、社会、环境密切相关,下列有关说法不正确的是( )
| A、PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康或环境有很大影响 |
| B、福岛核电站泄漏的放射性物质131I和127I互为同位素,化学性质几乎相同 |
| C、在黑夜中,我们能看到一束汽车的灯光,是因为我们生活中的大气是胶体体系 |
| D、铝制品在空气中不易被腐蚀是因为铝的性质不活泼 |
 Ⅰ、某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%.
Ⅰ、某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%.