题目内容
下列表达式中正确的是( )
A、氯化氢分子的电子式: | ||
B、S2-的结构示意图: | ||
C、O-18的原子符号:
| ||
| D、N2分子的结构式:N=N |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氯化氢为共价化合物,分子中不存在阴阳离子;
B.硫离子最外层为8个电子,核外电子总数为18;
C.氧元素的质子数为8,该氧原子的质量数为18;
D.氮气分子或者存在氮氮三键,不是氮氮双键.
B.硫离子最外层为8个电子,核外电子总数为18;
C.氧元素的质子数为8,该氧原子的质量数为18;
D.氮气分子或者存在氮氮三键,不是氮氮双键.
解答:
解:A.氯化氢分子中不存在阴阳离子,不能变成离子电荷,氯化氢正确的电子式为: ,故A错误;
,故A错误;
B.硫离子的核电荷数为16,核外电子总数为18,硫离子正确的结构示意图为: ,故B错误;
,故B错误;
C.O-18的质子数为8,质量数为18,该氧原子的原子符号为:
O,故C正确;
D.氮气分子的电子式为: ,将共用电子对换成短线即为结构式,氮气的结构式为:N≡N,故D错误;
,将共用电子对换成短线即为结构式,氮气的结构式为:N≡N,故D错误;
故选C.
 ,故A错误;
,故A错误;B.硫离子的核电荷数为16,核外电子总数为18,硫离子正确的结构示意图为:
 ,故B错误;
,故B错误;C.O-18的质子数为8,质量数为18,该氧原子的原子符号为:
18 8 |
D.氮气分子的电子式为:
 ,将共用电子对换成短线即为结构式,氮气的结构式为:N≡N,故D错误;
,将共用电子对换成短线即为结构式,氮气的结构式为:N≡N,故D错误;故选C.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握电子式、离子结构示意图、原子符号、结构式的概念及表示方法,明确离子化合物的与共价化合物的电子式的区别.

练习册系列答案
相关题目
下列各组离子一定能够大量共存的是( )
| A、使紫色石蕊变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| B、含有较多A13+的溶液:SO42-、Na+、Mg2+、NO3- |
| C、含有较多Fe3+的溶液:Na+、SO42-、SCN-、CO32- |
| D、无色透明的酸性溶液:MnO4-、K+、Cl-、HCO3- |
一定量的某有机物完全燃烧后,将燃烧产物通过足量的石灰水,经过滤可得沉淀10g,有机物燃烧产生2.7g水,则此有机物不可能是( )
| A、乙烷 | B、乙烯 | C、乙醇 | D、乙二醇 |
等物质的量的氢气和氦气具有相同的( )
| A、质量 | B、原子数 |
| C、质子数 | D、体积 |

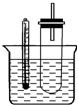 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.


