题目内容
2.已知X、Y为同周期元素,且第一电离能X<Y,下列说法中正确的是( )| A. | 电负性:X<Y | |
| B. | 周期表中,X可能在Y的右边 | |
| C. | 若X与Y形成化合物,则X显正价,Y显负价 | |
| D. | 气态氢化物的稳定性:HmY强于HnX |
分析 X、Y为同周期元素,且第一电离能X<Y,同周期随原子序数增大,第一电离能呈增大趋势,但ⅡA族、ⅤA族元素第一电离能大于同周期相邻元素,故则原子序数X<Y或X>Y.
A.同周期随原子序数增大,电负性增大;
B.ⅡA族、ⅤA族元素第一电离能高于同周期相邻元素;
C.电负性大的元素原子对键合电子吸引力更大,化合物中显负价;
D.非金属性越强,气态氢化物越稳定.
解答 解:X、Y为同周期元素,且第一电离能X<Y,同周期随原子序数增大,第一电离能呈增大趋势,但ⅡA族、ⅤA族元素第一电离能共有同周期相邻元素,故则原子序数X<Y或X>Y.
A.原子序数可能是X<Y或X>Y,同周期随原子序数增大,电负性增大,故电负性:X<Y或X>Y,故A错误;
B.由于ⅡA族、ⅤA族元素第一电离能高于同周期相邻元素,周期表中,X可能在Y的右边,也可能在Y的左边,故B正确;
C.电负性可能为:X<Y或X>Y,电负性大的元素原子对键合电子吸引力更大,化合物中显负价,故X与Y形成化合物中X显正价、Y显负价或X显负价、Y显正极,故C错误;
D.同周期自左而右非金属性增强,故非金属性:可能是X<Y或X>Y,非金属性越强,气态氢化物越稳定,故气态氢化物的稳定性:HmY强于HnX或HmY弱于HnX,故D错误,
故选B.
点评 本题考查位置结构性质关系应用,侧重对电离能的考查,注意理解掌握同周期元素第一电离能异常情况,学生容易忽略“ⅡA族、ⅤA族元素第一电离能高于同周期相邻元素”,属于易错题目,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列关系的表述中,正确的是( )
| A. | 已知草酸氢钾溶液呈酸性,则在amol•L-1 KHC2O4溶液中,c(C2O42-)<c(H2C2O4) | |
| B. | 新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) | |
| C. | 0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) | |
| D. | pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)相等 |
13.减少CO2的排放以及CO2的资源化利用具有重要意义.
(1)用氨水捕集烟气中的CO2生成铵盐,是减少CO2排放的可行措施之一.
①写出氨水捕集烟气中的CO2生成铵盐的主要化学方程式CO2+NH3•H2O═NH4HCO3.
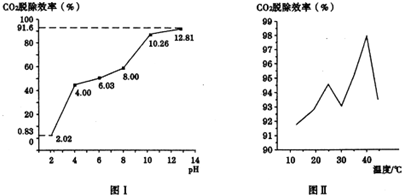
②分别用不同pH的吸收剂吸收烟气中的CO2,CO2脱除效率与吸收剂的pH关系如图Ⅰ所示,CO2脱除效率与吸收剂的pH关系是CO2脱除效率随吸收剂的pH增大而增大.烟气中CO2的含量为12%,烟气通人氨水的流量为0.052m3/h(标准状况),用pH为12.81的氨水吸收烟气30min,脱除的CO2的物质的量为0.13mol(精确到0.01).
③CO2脱除效率与温度的关系如图Ⅱ所示.从40℃到45℃脱除CO2效率降低的主要原因是碳酸氢铵受热易分解生成二氧化碳.
(2)将CO2和甲烷重整制合成气(CO和H2)是CO2资源化利用的有效途径.合成气用于制备甲醇的反应为
2H2(g)+CO(g)?CH3OH(g)△H=-90.1kJ/mol.
①在T℃时,容积相同的甲、乙、丙三个恒容密闭容器中,按不同方式投人反应物,测得反应达到平衡时的有关数据如下.
下列说法正确的是D(填字母編号).
A.2c1>c3 B.|x|+|y|<90.1 C.2p2<p3 D.a1+a3<1
②在T℃、恒容条件下,该反应的平衡常数Kp=6.0×10-3(kPa)-2.若甲容器中反应达到平衡时p(CH3OH)=24.0kPa,则平衡混合气体中CH3OH的物质的量分数为44.4%(Kp是用平衡分压代替平衡浓度计算所得平衡常数,分压=总压×物质的量分数).
(1)用氨水捕集烟气中的CO2生成铵盐,是减少CO2排放的可行措施之一.
①写出氨水捕集烟气中的CO2生成铵盐的主要化学方程式CO2+NH3•H2O═NH4HCO3.
②分别用不同pH的吸收剂吸收烟气中的CO2,CO2脱除效率与吸收剂的pH关系如图Ⅰ所示,CO2脱除效率与吸收剂的pH关系是CO2脱除效率随吸收剂的pH增大而增大.烟气中CO2的含量为12%,烟气通人氨水的流量为0.052m3/h(标准状况),用pH为12.81的氨水吸收烟气30min,脱除的CO2的物质的量为0.13mol(精确到0.01).
③CO2脱除效率与温度的关系如图Ⅱ所示.从40℃到45℃脱除CO2效率降低的主要原因是碳酸氢铵受热易分解生成二氧化碳.
(2)将CO2和甲烷重整制合成气(CO和H2)是CO2资源化利用的有效途径.合成气用于制备甲醇的反应为
2H2(g)+CO(g)?CH3OH(g)△H=-90.1kJ/mol.
①在T℃时,容积相同的甲、乙、丙三个恒容密闭容器中,按不同方式投人反应物,测得反应达到平衡时的有关数据如下.
| 容器 | 甲 | 乙 | 丙 | |
| 起始反应物投入量 | 2mol H2、l mol CO | 1mol CH3OH | 2mol CH3OH | |
| 平 | c(CH,0H)/mol/L | C1 | C2 | c3 |
| 衡 | 反应的能量变化ZkJ | x | y | z |
| 数 | 体系压强/Pa | P1 | P2 | P3 |
| 据 | 反应物转化率 | a1 | a2 | a3 |
A.2c1>c3 B.|x|+|y|<90.1 C.2p2<p3 D.a1+a3<1
②在T℃、恒容条件下,该反应的平衡常数Kp=6.0×10-3(kPa)-2.若甲容器中反应达到平衡时p(CH3OH)=24.0kPa,则平衡混合气体中CH3OH的物质的量分数为44.4%(Kp是用平衡分压代替平衡浓度计算所得平衡常数,分压=总压×物质的量分数).

10.元素周期表的一部分,回答下列问题(用元素符号填写):
(1)分别写出①、③两种元素形成的高价态化合物的电子式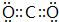
(2)写出⑨的原子结构示意图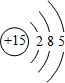 .
.
(3)在这些元素中,最活泼的金属元素的最高价氧化物对应水化物的电子式为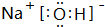 含有化学键为离子键、共价键
含有化学键为离子键、共价键
(4)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;形成两性氢氧化物的化学式是Al(OH)3;上述两者反应的离子方程式Al(OH)3+3H+═Al3++3H2O
(5)从⑤到(11)的元素中,Cl原子半径最小.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VIIA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | (10) | (11) | (12) |
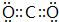
(2)写出⑨的原子结构示意图
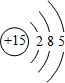 .
.(3)在这些元素中,最活泼的金属元素的最高价氧化物对应水化物的电子式为
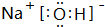 含有化学键为离子键、共价键
含有化学键为离子键、共价键(4)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;形成两性氢氧化物的化学式是Al(OH)3;上述两者反应的离子方程式Al(OH)3+3H+═Al3++3H2O
(5)从⑤到(11)的元素中,Cl原子半径最小.
7.Y、Z三种金属,X、Y组成原电池,X是负极;把Z放入X的硝酸盐溶液中,Z表面有X析 出.三者的金属活动性顺序是( )
| A. | X>Y>Z | B. | Z>X>Y | C. | X>Z>Y | D. | Y>X>Z |
11.下列各组性质的比较,正确的是( )
| A. | 原子半径:Na<Mg<Al | B. | 酸性强弱:H2CO3<H2SiO3<HNO3 | ||
| C. | 热稳定性:HF>HCl>HBr | D. | 非金属性强弱:P>S>Cl |
12.根据元素周期表,下列叙述正确的是( )
| A. | 钾与钠同一主族,钠比钾更容易从水中置换出氢 | |
| B. | 溴化钾与碘化钾溶液置于空气中,溴化钾更容易被氧化 | |
| C. | 过渡元素都是副族元素 | |
| D. | 同周期元素的原子,半径越大,越容易失去电子 |
 ,元素B在周期表中的位置2周期ⅥA族.
,元素B在周期表中的位置2周期ⅥA族.