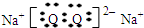题目内容
在2Na2O2+2H2O=4NaOH+O2↑化学反应中,Na2O2所起的作用是( )
分析:在2Na2O2+2H2O=4NaOH+O2↑化学反应中,Na2O2中O元素的化合价由-1价变为0价和-2价,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,据此分析解答.
解答:解:在2Na2O2+2H2O=4NaOH+O2↑化学反应中,Na2O2中O元素的化合价由-1价变为0价和-2价,该反应中过氧化钠既得电子又失电子,所以过氧化钠既是氧化剂又是还原剂,故选C.
点评:本题考查了氧化还原反应,明确元素化合价变化是解本题关键,根据得失电子判断氧化剂、还原剂,难度不大.

练习册系列答案
相关题目