��Ŀ����
��ͼ��298K ʱN2��H2��Ӧ�����������仯������ͼ������������ȷ���� ( )
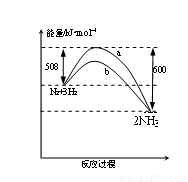
A. �÷�Ӧ���Ȼ�ѧ����ʽΪ��
N2(g) + 3H2(g)  2NH3(g)
��H = 92kJ��mol-1
2NH3(g)
��H = 92kJ��mol-1
B.b�����������¶�ʱ�������仯����
C. �������, �û�ѧ��Ӧ�Ļ�ܺͷ�Ӧ�ȶ��ı�
D. ���¶����һ����������, ͨ��lmol N2��3molH2 ��Ӧ��ų�������ΪQ1kJ, ��ͨ��2mol N2��6mol H2 ��Ӧ��ų�������ΪQ2kJ ��184>Q2 >2Q1
D
��������A����H Ӧ�����ű�ʾ���ȣ�B��b�����Dz�ʹ�ô���ʱ�������仯���ߣ�C���������ʱ����Ӧ�Ļ�ܽ��ͣ�����Ӧ�Ȳ��䣻D�����淴Ӧ�����ܽ��е��ף�������ʽ֪��ͨ��2mol N2��6mol H2 ���ų���������Q2 <184kJ�����ں�������£��൱��������ͨ��lmol N2��3molH2�Ҽ�ѹ������Q2 >2Q1��ѡ����ȷ���ʴ�ΪD

 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�����һ����ѧ��Ӧ���о���Ҫ�ӷ�Ӧ�������ȡ����ʡ�������ϵ�����ؽ����ۺϷ����������ǹ��ڻ�ѧ��Ӧ��ϵ���о�������������Ϣ�ش����⡣
�Ź��ڷ�Ӧ��֮��Ķ�����ϵ���о���
��֪��Ӧ��Br2 +2Fe2+=2 Br -+2Fe3+,��10 mL0 .1mol/L��Fe Br2��Һ��ͨ��0 .003mol Cl2���÷�Ӧ�����ӷ���ʽΪ
�ƹ��ڷ�Ӧ���ʡ��ȵ��о���
����֪298Kʱ��Mg(OH)2���ܶȻ�����Ksp��5.6��10��12�����Ȼ�þ��Һ�м���һ�������ռ���pH=13.0,����¶��²�������Һ�е�c(Mg 2+)��
�ڿ�ѧ�о�����������Cu2O����Ϊ̫����ֽ�ˮ�Ĵ�����
һ���¶��£���2L�ܱ������м���������Cu2O��ͨ��0 .1molˮ������������Ӧ��
 2 H2O(g)
2 H2O(g)
2 H2 (g) + O2(g) ��H��+484kJ�� mol-1����ͬʱ�β���O2�������±���
|
ʱ��/min |
20 |
40 |
60 |
80 |
|
n(O2)/mol |
0.0010 |
0.0016 |
0.0020 |
0.0020 |
��ǰ20min�ķ�Ӧ����v(H2O)= ���ﵽƽ��ʱ��������Ҫ���յĹ���Ϊ kJ��
����ij�ܱ������м���0 .3molA��0 .1molC��һ������B�������塣һ�������·�����Ӧ��������Ũ����ʱ��仯����ͼ�м�ͼ��ʾ����ͼ����ͼΪt2ʱ�̺�ı�������������ƽ����ϵ�з�Ӧ������ʱ��仯����������ĸ��ζ�ֻ�ı�һ����������֪t3��t4Ϊʹ�ô�������ͼ��t0��t1��c (B)δ��������ش�

��t4��t5�θı�������� t5��t6�θı��������
��B����ʼŨ��Ϊ ���÷�Ӧ����ʽΪ
��08ɽ��ʡ�������ʼ죩��8�֣�I����1����֪298Kʱ2C��s��+O2��g��=2CO(g) ��H1=��221.01kJ?mol��1
C��s��+O2��g��=CO2(g) ��H2=��393.5kJ?mol��1 ��298KʱCO(g)��O2(g)ȼ������CO2(g) ���Ȼ�ѧ��Ӧ����ʽΪ��________��
��2��һ�����͵�������ȼ�ϵ�ؾ��и߷���Ч�ʶ��������ӡ�����Li2CO3��Na2CO3�������λ����������ʣ�һ��ͨ��CO���壬��һ��ͨ�������CO2�Ļ�����壬�Ƶ�ȼ�ϵ�ء�
�õ�ع���ʱ�ĸ�����ӦʽΪ�� ��
��������CO32�������ʵ����ڹ���ʱ ������������١��������䡱����
|
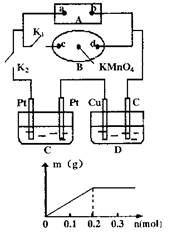
II������ͼ��ʾ��AΪ��Դ��BΪ������ʳ��ˮ�ͷ�̪��Һ����ֽ����ֽ�������һ��KMnO4��Һ��C��D
Ϊ���ۣ���缫���ϼ��������Һ��ͼ��
��1���ر�K1����K2��ͨ���B��KMnO4�Ϻ�ɫҺ����c���ƶ������Դa��Ϊ ����ͨ��һ��ʱ��۲쵽��ֽd�˳��ֵ������ǣ� ��
��2����֪Cװ������ҺΪCu(NO3)2��X��NO3��3���Ҿ�Ϊ0.1mol����K1���ر�K2��ͨ��һ��ʱ�������������������m(g)��ͨ�����ӵ����ʵ���n(mol)��ϵ��ͼ��ʾ����Cu2+��X3+��H+���������ɴ�С��˳���� ��Dװ��Cu���ĵ缫��ӦʽΪ ��
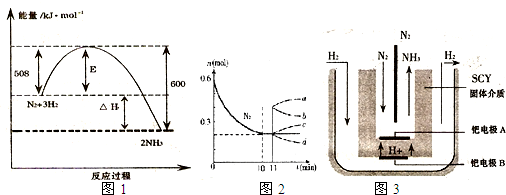

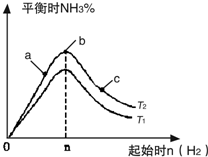 ����N2��H2����ʵ��NH3�Ĺ�ҵ�ϳɣ������ֿ��Խ�һ���Ʊ����ᣬ�ڹ�ҵ��һ��ɽ���������������ش��������⣺
����N2��H2����ʵ��NH3�Ĺ�ҵ�ϳɣ������ֿ��Խ�һ���Ʊ����ᣬ�ڹ�ҵ��һ��ɽ���������������ش��������⣺