题目内容
17.标准状况下,CO2分子数为6.02×1023,CO2的物质的量为1mol,CO2的质量为44g,CO2的体积为22.4L.分析 根据n=$\frac{N}{{N}_{A}}$计算出二氧化碳的物质的量,根据m=nM计算出该二氧化碳的质量,最后根据V=nVm计算出二氧化碳在标准状况下的体积.
解答 解:CO2分子数为6.02×1023,CO2的物质的量为:n(CO2)=$\frac{6.03×1{0}^{23}}{6.03×1{0}^{23}mo{l}^{-1}}$=1mol,1mol 该二氧化碳的质量为:44g/mol×1mol=44g,标准状况下1mol CO2的体积为:22.4L/mol×1mol=22.4L,
故答案为:1mol;44g;22.4L.
点评 本题考查了物质的量的简单计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积、阿伏伽德罗常数等物理量之间的关系即可解答,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
13.将浓度为0.1mol•L-1的氨水加水不断稀释,下列各量始终保持减小的是( )
| A. | Kb(NH3•H2O) | B. | n(OH-) | C. | $\frac{{c({N{H_3}•{H_2}O})}}{{c({O{H^-}})}}$ | D. | $\frac{{c({O{H^-}})}}{{c({NH_4^+})}}$ |
8.工业上常用煤和水作原料经过多步反应制得氢气,其中一步的反应原理为:
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g)下面选项的条件中可判断该反应达到平衡状态的是( )
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g)下面选项的条件中可判断该反应达到平衡状态的是( )
| A. | 单位对间内消耗2mol的CO同时生成2mol的CO2 | |
| B. | 两个H-O键断裂的同时有一个H-H键断裂 | |
| C. | 反应容器内的压强不再发生变化 | |
| D. | 混合气体的相对分子质量不发生变化 |
5.若某甲原子(质子数为10)质量是a g,C-12的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是( )
| A. | 甲元素的相对原子质量一定是$\frac{12a}{b}$ | |
| B. | 该甲原子的摩尔质量是aNAg | |
| C. | Wg该甲原子的物质的量一定是Wa/(NA)mol | |
| D. | Wg该甲原子所含质子数是10W/a |
12.在碱性溶液中能大量共存且为无色透明的溶液是( )
| A. | K+、Cl-、MnO4-、SO42- | B. | Na+、K+、NO3-、CO32- | ||
| C. | Na+、NO3-、SO42-、HCO3- | D. | Na+、SO42-、H+、Cl- |
2.下列说法中,正确的是( )
| A. | Na2O、Na2O2为相同元素组成的金属氧化物,其中Na2O2不属于碱性氧化物 | |
| B. | SiO2是硅酸的酸酐,NO2是HNO3的酸酐 | |
| C. | Fe(OH)3与氢碘酸反应的类型为复分解反应 | |
| D. | 将Fe(OH)3胶体和泥水分别进行过滤,分散质均不能通过滤纸孔隙 |
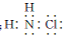 .
.