题目内容
5.若某甲原子(质子数为10)质量是a g,C-12的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是( )| A. | 甲元素的相对原子质量一定是$\frac{12a}{b}$ | |
| B. | 该甲原子的摩尔质量是aNAg | |
| C. | Wg该甲原子的物质的量一定是Wa/(NA)mol | |
| D. | Wg该甲原子所含质子数是10W/a |
分析 A.根据原子相对原子质量是等于原子的质量除以碳原子质量的$\frac{1}{12}$计算;
B.摩尔质量的单位是g/mol;
C.依据物质的量n=$\frac{m}{M}$计算Wg该甲原子的物质的量;
D.该原子的质子数为10,根据N=nNA计算含有质子数.
解答 解:A.原子相对原子质量是等于原子的质量除以碳原子质量的$\frac{1}{12}$,该原子的相对原子质量=$\frac{12a}{b}$,故A正确;
B.该原子的摩尔质量是aNA g/mol,故B错误;
C.Wg该原子的物质的量为:$\frac{Wg}{a{N}_{A}g/mol}$=$\frac{W}{a{N}_{A}}$mol,故C错误;
D.Wg该原子所含质子数:$\frac{Wg}{a{N}_{A}g/mol}$×10NA=$\frac{10W}{a}$,故D正确;
故选AD.
点评 本题考查了物质的量的计算,题目难度中等,相对原子质量的概念及计算方法为解答关键,注意熟练掌握物质的量与其它物理量之间的关系,试题有利于提高学生的化学计算能力.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
1.在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A. | Na+、K+、OH-、Cl- | B. | Cu2+、Cl-、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ca2+、HCO3-、NO3-、K+ |
13.下列叙述正确的是( )
| A. | 同温同压下,相同体积的物质,它们的物质的量一定相等 | |
| B. | 任何条件下,等质量的一氧化二氮(N2O)和二氧化碳所含的分子数必相等 | |
| C. | 1 L一氧化碳的质量一定比1 L氧气质量小 | |
| D. | 等体积、等物质的量浓度的盐酸和硫酸中所含的H+数一定相等 |
20.某温度下,测得某医用钢瓶中有22.4LO2,下列叙述正确的是( )
| A. | 它的质量是32 g | B. | 约含有6.02×1023个O2分子 | ||
| C. | 含有2 mol O | D. | 红热的铁丝可在其中剧烈燃烧 |
10.下列说法不正确的是( )
| A. | ${\;}_{6}^{14}$C表示质子数为6、中子数为8的核素 | |
| B. | 甲醇(CH3OH)和甘油( 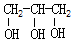 )互为同系物 )互为同系物 | |
| C. | C5H12的同分异构体有3种,其沸点各不相同 | |
| D. | CH3CH2CH2CH(CH3)2的名称是2-甲基戊烷' |
15.下列变化不能用勒夏特列原理解释的是( )
| A. | 氯水宜保存在低温、避光条件下 | |
| B. | H2、I2、HI混合气体加压后颜色变深 | |
| C. | SO2催化氧化成SO3的反应,往往加入过量的空气 | |
| D. | 打开汽水瓶,看到有大量的气泡逸出 |