题目内容
1.氯化两面针碱(H)具有抑制肿瘤细胞增殖和诱杀作用,被认定为潜在的抗肿瘤药物.其合成路线如图: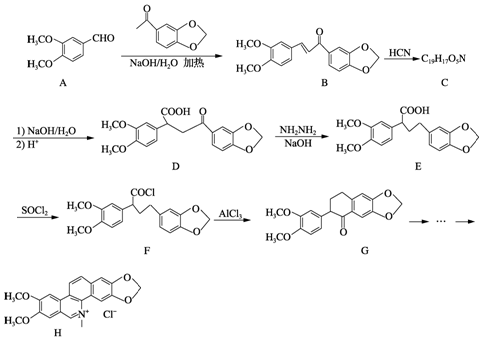
(1)化合物B中含氧官能团的名称为羰基和醚键.
(2)化合物C的结构简式为
 ;由E→F的反应类型为取代.
;由E→F的反应类型为取代.(3)写出同时满足下列条件的A的一种同分异构体的结构简式
 .
.①能与FeCl3溶液发生显色反应,②既能发生银镜反应又能发生水解反应;③分子中只含4种不同化学环境的氢.
(4)请以CH2ClCH2CH2CH2OH为原料制备
 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
分析 比较A、B结构简式知,A发生取代反应生成B,比较B和D的结构简式可知,结合C的分子式可知,B发生加成反应生成C,C为 ,D发生取代反应生成E,E发生取代反应生成F,F发生消去反应生成G,G发生一系列反应生成H;
,D发生取代反应生成E,E发生取代反应生成F,F发生消去反应生成G,G发生一系列反应生成H;
(4)CH2ClCH2CH2CH2OH发生催化氧化反应生成CH2ClCH2CH2CHO,CH2ClCH2CH2CHO发生氧化反应生成
CH2ClCH2CH2COOH,CH2ClCH2CH2COOH发生水解反应生成HOCHCH22CH2COOH,HOCH2CH2CH2COOH发生分子内酯化即可得到目标产物.
解答 解:(1)由B的结构简式 可知分子结构中含有的含氧官能团为羰基和醚键,故答案为:羰基和醚键;
可知分子结构中含有的含氧官能团为羰基和醚键,故答案为:羰基和醚键;
(2)由分析可知C的结构简式为 ,由E发生取代反应生成F,故答案为:
,由E发生取代反应生成F,故答案为: ;取代;
;取代;
(3)①能与FeCl3溶液发生显色反应,说明含有苯环和酚羟基;②既能发生银镜反应又能发生水解反应,说明含有醛基和酯基,可能是甲酸酯;③分子中只含4种不同化学环境的氢,说明结构对称性比较强,符合上述条件的A的同分异构体可能是 ,故答案为:
,故答案为: ;
;
(4)以CH2ClCH2CH2CH2OH为原料制备 的合成流程为:
的合成流程为: ;
;
故答案为: .
.
点评 本题考查有机推断与合成,涉及多官能团有机物性质及同分异构体的书写,难点是设计合成路线以原料合成目标产物,综合性较强,对学生基础性知识要求较高,中等难度.

练习册系列答案
相关题目
7.下列叙述正确的是( )
| A. | 在原电池的负极和电解池的阴极上都发生失电子的氧化反应 | |
| B. | 用惰性电极电解饱和NaCl溶液,若有0.1 mol电子转移,则生成0.1 mol NaOH | |
| C. | 用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 | |
| D. | 镀层破损后,镀锌铁板比镀锡铁板更易腐蚀 |
8.下列各组离子一定可以大量共存的是( )
| A. | 加铝粉产生H2的溶液:Fe2+、K+、Cl-、NO3- | |
| B. | 能使紫色石蕊试液变蓝的溶液:Na+、S2-、SiO32-、SO42- | |
| C. | 由水电离出的c(H+)=1×10-12 mol/L的溶液:Ca2+、HCO3-、Br-、S2- | |
| D. | 遇KSCN变红色的溶液:NH4+、AlO2-、I-、CO32- |
5.在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g);△H=-373.2kJ•mol-1
达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A. | 加催化剂同时升高温度 | B. | 加催化剂同时增大压强 | ||
| C. | 升高温度同时充入N2 | D. | 降低温度同时减小压强 |
12.将等体积、等pH的NaOH溶液和NH3•H2O溶液,分别加入到盛有10mL1mol/LAlCl3溶液的甲、乙两烧杯中.下列说法正确的是( )
| A. | 甲中沉淀一定比乙多 | B. | 甲和乙中沉淀可能一样多 | ||
| C. | 甲中沉淀可能比乙多 | D. | 乙中沉淀一定比甲多 |
6. 一定温度下,在三个容积为2.0L的恒容密闭容器中发生反应:
一定温度下,在三个容积为2.0L的恒容密闭容器中发生反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g)
各容器中起始物质的量浓度与反应温度如表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示.
下列说法正确的是( )
 一定温度下,在三个容积为2.0L的恒容密闭容器中发生反应:
一定温度下,在三个容积为2.0L的恒容密闭容器中发生反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)
各容器中起始物质的量浓度与反应温度如表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示.
| 容器 | 温度/℃ | 起始物质的量浓度/mol•L-1 | |||
| NO (g) | CO (g) | N2(g) | CO2(g) | ||
| 甲 | T1 | 0.10 | 0.10 | 0 | 0 |
| 乙 | T2 | 0 | 0 | 0.10 | 0.20 |
| 丙 | T2 | 0.10 | 0.10 | 0 | 0 |
| A. | 该反应的正反应为吸热反应 | |
| B. | 乙容器中反应达到平衡时,N2的转化率小于40% | |
| C. | 达到平衡时,乙容器中的压强一定大于甲容器的2倍 | |
| D. | 丙容器中反应达到平衡后,再充入0.10mol NO和0.10mol CO2,此时v(正)<v(逆) |
10.室温下,将1mol的CuSO4•5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol 的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2,CuSO4•5H2O 受热分解的化学方程式为:CuSO4•5H2O(s)$\frac{\underline{\;△\;}}{\;}$CuSO4(s)+5H2O(l),热效应为△H3.则下列判断正确的是( )
| A. | △H2>△H3 | B. | △H1>△H3 | C. | △H1+△H3=△H2 | D. | △H1+△H2<△H3 |
11.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 钠在空气中燃烧可生成多种氧化物,23 g钠充分燃烧时转移电子数为NA | |
| B. | 1 L 0.1 mol/L的NaHCO3溶液中HCO3-离子数为0.1 NA | |
| C. | 1L pH=1的稀硫酸中有0.2 NA个H+ | |
| D. | 标准状况下,22.4L氯仿(三氯甲烷)中共价键数目为4NA |

 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$
 .
. .
. ),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):