题目内容
9.下列反应中氧化剂与还原剂物质的量之比为2:1的是( )| A. | 2H2S+SO2→3S+2H2O | B. | 3NO2+H2O→2HNO3+NO | ||
| C. | Fe+2FeCl3→3FeCl2 | D. | 2H2S+O2→2S↓+2H2O |
分析 A、2H2S+SO2→3S+2H2O,氧化剂是二氧化硫,还原剂是硫化氢;
B、3NO2+H2O→2HNO3+NO,二氧化氮既是氧化剂也是还原剂;
C、Fe+2FeCl3→3FeCl2铁是还原剂,氯化铁是氧化剂;
D、2H2S+O2→2S↓+2H2O中硫化氢是还原剂,氧气是氧化剂.
解答 解:A、2H2S+SO2→3S+2H2O,氧化剂是二氧化硫,还原剂是硫化氢,氧化剂与还原剂物质的量之比为1:2,故A不符合;
B、3NO2+H2O→2HNO3+NO,二氧化氮既是氧化剂也是还原剂,氧化剂与还原剂物质的量之比为1:2,故B不符合;
C、Fe+2FeCl3→3FeCl2铁是还原剂,氯化铁是氧化剂,氧化剂与还原剂物质的量之比为2:1,故C符合;
D、2H2S+O2→2S↓+2H2O中硫化氢是还原剂,氧气是氧化剂,氧化剂与还原剂物质的量之比为1:2,故D不符合;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念和转移电子的考查,题目难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
17.设 NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 将 78gNa2O2 与过量 CO2反应转移的电子数为 2NA | |
| B. | 1mol N2与 4mol H2反应生成的 NH3 分子数为 2NA | |
| C. | 标准状况下,2.24L SO3 中所含原子数为 0.4 NA | |
| D. | 标准状况下,18g D2O 中所含电子数为 9 NA |
14.“瓦斯”爆炸会严重威胁煤矿安全,下列说法正确的是( )
| A. | “瓦斯”的主要成分为一氧化碳 | B. | 爆炸过程放出大量热量 | ||
| C. | 爆炸过程有氧气参与反应 | D. | 爆炸过程吸收大量热量 |
18.下列关于物质分类的说法正确的是( )
| A. | 金属氧化物都是碱性氧化物 | |
| B. | 氨水和液氯都是纯净物 | |
| C. | CuSO4溶液和Al(OH)3胶体都能产生丁达尔效应 | |
| D. | 碳酸氢钠属于盐类 |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,将22.4L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA | |
| B. | 常温常压下,16gCH4所含中子数目为8NA | |
| C. | 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA | |
| D. | 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
 2015年11月首架C919打飞机总装下线,标志着我国跻身飞机研制先进国家行列.
2015年11月首架C919打飞机总装下线,标志着我国跻身飞机研制先进国家行列.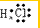 ;由两种元素组成的共价化合物的水溶液显碱性,这种化合物的结构式是
;由两种元素组成的共价化合物的水溶液显碱性,这种化合物的结构式是 .
.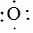 →
→ .
.