题目内容
【题目】下列关于碳酸(H2CO3)和硅酸(H2SiO3)的说法中不正确的是( )
A. 两者均为弱酸
B. 两者均可使紫色石蕊试液变红色
C. CO2气体通入Na2SiO3溶液中可以制得硅酸
D. 两者受热时均可以分解
【答案】B
【解析】硅酸不能够使紫色石蕊试液变红,B错误。

【题目】氨的合成是人类科学技术上的一项重大突破。其原理如下:
N2( g) +3H2( g) ![]() 2NH3( g) △H= -92.4kJ/mol
2NH3( g) △H= -92.4kJ/mol
据此回答下列与NH3有关的问题:
(1)该反应的化学平衡常数表达式为K =_________ 。
(2)①500℃时,若把10molN2与20molH2置于体积为10L的密闭容器内,测得容器内压强随时间的变化关系如下表:
压强/MPa | 9.6 | 8.4 | 7.6 | 7.0 | 6.4 | 6.4 | 6.4 | 6.4 |
时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
则从反应开始到平衡这段时间内,v(H2)=_________mol/(L·min)。若达到平衡后,再充人5mol N2与10molH2,再次达到平衡时NH3的体积分数与原平衡状态相比_____(填“增大”“减小”或“不变”)。
②合成氨反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(p1、p2)下随温度变化的曲线,下列图示正确的是_____(填“A”或“B”);比较p1、p2的大小关系:_____________。

③某温度下,在恒压的某密闭容器中投入等物质的量的N2和H2,一段时间后测得H2的体积分数为40%,之后保持不变,则达到平衡时H2的转化率为________________。
(3)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料,与水在一定条件下可以生成氨气:
CO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g) △H = +133.6kJ/mol。关于该反应,下列说法正确的
2NH3(g)+CO2(g) △H = +133.6kJ/mol。关于该反应,下列说法正确的
是______(填序号)。
a.从反应开始到达到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中再加入少量CO(NH2)2,平衡正向移动
c.降低温度使尿素的转化率减小
d.恒温恒容时,向平衡体系中再充人少量氨气,平衡常数减小
(4)将氨气溶于水得到氨水,是一种弱碱。常温下,现将amol/L氨水和0.01mol/L盐酸等体积混合后,溶液中c(NH4+)=c(Cl-),则氨水的Kb=_____________。(用含a的代数式表示)
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HC1O |
电离平衡常数 | 1.7×10-5 | K1=4.3×10 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH、H2CO3、HC1O的酸性由强到弱的顺序为______________________。
(2)写出H2CO3的电离方程式:______________________。
(3)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是______________________(填宇母序号,下同)。
A.c(H+) B.c(H+)/c(CH3COOH)
C. c(H+)·c(OH-) D. 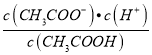
若该溶液升髙温度,上述4种表达式的数据增大的是_________________________。
(4)取0.10mol CH3COOH (冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示:比较a、b点的相关性质(填“>”“<”或“=”):
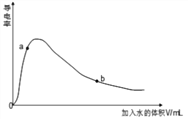
n(H+)∶a_____b;c(CH3COO-)∶a_____b;完全中和时消耗NaOH的物质的量∶a_____b;
(5)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分別与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同, 则下列说法正确的是__________(填写序号)
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④A中有锌剩余