题目内容
5.下列说法正确的是(设阿伏加德罗常数的数值为NA)( )| A. | 在标准状况下,22.4L水所含分子数目为NA | |
| B. | 1mol•L-1 K2SO4溶液所含K+数目为2NA | |
| C. | 1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA | |
| D. | O2的摩尔体积约为22.4 L•mol-1 |
分析 A、标况下水为液体;
B、溶液体积不明确;
C、钠反应后变为+1价;
D、气体摩尔体积和状态有关.
解答 解:A、标况下水为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、溶液体积不明确,故溶液中的钾离子的个数无法计算,故B错误;
C、钠反应后变为+1价,故1mol钠反应后失去NA个电子,与产物无关,故C正确;
D、气体摩尔体积和状态有关,与气体的种类无关,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列各组离子在给定条件的溶液中可能大量共存的是( )
| A. | 加入铝粉有大量氢气产生的溶液中:Ca2+、K+、NO3-、Cl- | |
| B. | PH=0的无色溶液中:Na+、K+、MnO4-、NO3- | |
| C. | 在0.1mol/L的盐酸中:Fe2+、Na+、ClO-、Ca2+ | |
| D. | 在含有大量Fe3+的溶液中:NH4+、Ca2+、Cl-、K+ |
10. 研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO 作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中正确的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO 作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中正确的是( )
 研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO 作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中正确的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO 作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中正确的是( )| A. | 将熔融CaF2-CaO 换成Ca 处理也可以达到相同目的 | |
| B. | 阳极的电极反应式为:C+2O2--4e-═CO2↑ | |
| C. | 在制备金属钛前后,整套装置中CaO 的总量减少 | |
| D. | 若用铅蓄电池作该装置的供电电源,“+”接线柱应连接Pb 电极 |
15.用NA表示阿伏伽德罗常数的值.下列判断正确的是( )
| A. | 1mol H2含有的分子数目为NA | |
| B. | 24g Mg变为Mg2+时失去的电子数目为NA | |
| C. | 1L 1mol•L-1CaCl2溶液中含有的Cl-离子数目为NA | |
| D. | 常温常压下,11.2LO2中含有的原子数目为NA |
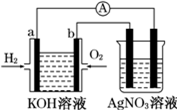 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.