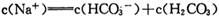��Ŀ����
��14�֣�������ĿҪ��ش��������⡣
��1�������£�Ũ�Ⱦ�Ϊ0.lmol��L-1������������Һ��pH���±���
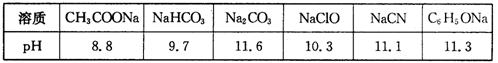
����������Һ�е������ӣ����H+������ǿ����
�ڸ��ݱ������ݣ�Ũ�Ⱦ�Ϊ0.0lmol��L-1�������������ʵ���Һ�У�������ǿ���� �����ţ���������Һ�ֱ�ϡ��100����pH�仯��С���� �����ţ�

�۾��ϱ����ݣ������ж����з�Ӧ���ܳ������� �����ţ�


��Ҫ������ˮ��HC1O��Ũ�ȣ�������ˮ�м���������̼��������Һ����Ӧ�����ӷ���ʽΪ ��
��2����֪������ ����֪������ijCuSO4��Һ��
����֪������ijCuSO4��Һ��
02 mol��L-1�����Ҫ����Cu��OH��2��������Ӧ������ҺpH����____��
��3����֪���淴Ӧ ��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���

��д���÷�Ӧƽ�ⳣ���ı���ʽ��____ ��
�����÷�Ӧ������̶����ܱ������н��У���һ�������´ﵽƽ��״̬���ı����������������¶ȣ����������ܶ� ��ѡ�������С�����䡱������ ���������ƽ����Է�������Ϊ ��
���������ƽ����Է�������Ϊ ��
��1�������£�Ũ�Ⱦ�Ϊ0.lmol��L-1������������Һ��pH���±���
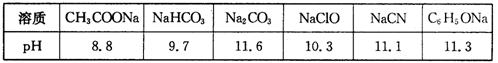
����������Һ�е������ӣ����H+������ǿ����
�ڸ��ݱ������ݣ�Ũ�Ⱦ�Ϊ0.0lmol��L-1�������������ʵ���Һ�У�������ǿ���� �����ţ���������Һ�ֱ�ϡ��100����pH�仯��С���� �����ţ�

�۾��ϱ����ݣ������ж����з�Ӧ���ܳ������� �����ţ�


��Ҫ������ˮ��HC1O��Ũ�ȣ�������ˮ�м���������̼��������Һ����Ӧ�����ӷ���ʽΪ ��
��2����֪������
 ����֪������ijCuSO4��Һ��
����֪������ijCuSO4��Һ��
02 mol��L-1�����Ҫ����Cu��OH��2��������Ӧ������ҺpH����____��
��3����֪���淴Ӧ
 ��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
��д���÷�Ӧƽ�ⳣ���ı���ʽ��____ ��
�����÷�Ӧ������̶����ܱ������н��У���һ�������´ﵽƽ��״̬���ı����������������¶ȣ����������ܶ� ��ѡ�������С�����䡱������
 ���������ƽ����Է�������Ϊ ��
���������ƽ����Է�������Ϊ ����14�֣���1����CO32-��2�֣���D��C ��2�֣� ��D��2�֣�
�� Cl2+HCO3-="=" CO2+Cl-+HClO ���ֲ���д���ո��֣���2�֣�
��2�� 5��2�֣�
��3����c��CO2��/c��CO����2�֣��ڼ�С��33��3��2�֣�
�� Cl2+HCO3-="=" CO2+Cl-+HClO ���ֲ���д���ո��֣���2�֣�
��2�� 5��2�֣�
��3����c��CO2��/c��CO����2�֣��ڼ�С��33��3��2�֣�
��1����������ˮ��Ӧ�á��ٸ��ݡ�Խ��Խˮ�⡱֪ʶ�㣬���ѵó�CO32-����ˮ��̶������ġ���ͬ�����ԱȽϵõ��������ǿ����С˳��Ӧ���ǣ�CH3COOH > H2CO3 > HClO > HCN > C6H5OH��ϡ��ͬ�����������£�����ԽС����仯ԽС����Dѡ���в����ϡ�ǿ�������ᡱ��ԭ��������ˮ�����ɵ�HCl��HClO��HCl���HCO3-����HClO�����HCO3-�����з�ӦӦ��ΪCl2+HCO3-="=" CO2+Cl-+HClO
��2����������ܽ�ƽ���Ӧ�á�Ksp[Cu(OH)2]=c(Cu2+)��c(OH��)2���� 02 mol��L-1��c(OH��)=1��10-9 mol��L-1����c(H��) =1��10-5mol��L-1������PHҪ����5
02 mol��L-1��c(OH��)=1��10-9 mol��L-1����c(H��) =1��10-5mol��L-1������PHҪ����5
��3������ƽ�ⳣ����ƽ���ƶ������ء��ٸ�ƽ����FeO��FeΪ���壬Ũ��Ϊһ��ֵ����K= c��CO2��/c��CO���������¶Ⱥ�ƽ�ⳣ��K��ϵ����֪��Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ���淽���ƶ������������ܶȼ�С���� ʱ��CO2ռ�����������1/3��COռ�����������2/3�����Ի������ƽ����Է�������Ϊ33��3
ʱ��CO2ռ�����������1/3��COռ�����������2/3�����Ի������ƽ����Է�������Ϊ33��3
��2����������ܽ�ƽ���Ӧ�á�Ksp[Cu(OH)2]=c(Cu2+)��c(OH��)2����
 02 mol��L-1��c(OH��)=1��10-9 mol��L-1����c(H��) =1��10-5mol��L-1������PHҪ����5
02 mol��L-1��c(OH��)=1��10-9 mol��L-1����c(H��) =1��10-5mol��L-1������PHҪ����5��3������ƽ�ⳣ����ƽ���ƶ������ء��ٸ�ƽ����FeO��FeΪ���壬Ũ��Ϊһ��ֵ����K= c��CO2��/c��CO���������¶Ⱥ�ƽ�ⳣ��K��ϵ����֪��Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ���淽���ƶ������������ܶȼ�С����
 ʱ��CO2ռ�����������1/3��COռ�����������2/3�����Ի������ƽ����Է�������Ϊ33��3
ʱ��CO2ռ�����������1/3��COռ�����������2/3�����Ի������ƽ����Է�������Ϊ33��3
��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ