题目内容
已知 25℃时有关弱酸的电离平衡常数:
则下列说法正确的是( )
A.等物质的量浓度的各溶液 pH 关系为:pH ( NaCN)>pH(Na2CO3)>pH( CH3COONa)
B.浓度均为0.2mol/LNaHCO3和 Na2CO3溶液中,存在的粒子种类不相同
C.0.4 mol·L-1HCN 溶液与 0.2 mol·L-1NaOH 溶液等体积混合后,所得溶液中:c(Na+)>c(OH-)>c(H+)
D.25℃时,pH=4且浓度均为0.1 mol·L-1的 CH3COOH、CH3COONa混合溶液中:
c(Na+)+c(H+)>c(CH3COO-)+c(CH3COOH)
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
A.等物质的量浓度的各溶液 pH 关系为:pH ( NaCN)>pH(Na2CO3)>pH( CH3COONa)
B.浓度均为0.2mol/LNaHCO3和 Na2CO3溶液中,存在的粒子种类不相同
C.0.4 mol·L-1HCN 溶液与 0.2 mol·L-1NaOH 溶液等体积混合后,所得溶液中:c(Na+)>c(OH-)>c(H+)
D.25℃时,pH=4且浓度均为0.1 mol·L-1的 CH3COOH、CH3COONa混合溶液中:
c(Na+)+c(H+)>c(CH3COO-)+c(CH3COOH)
C
由所给电离平衡常数知,酸性:CH3COOH>H2CO3>HCN>HCO3—
A项:越弱越水解,可知等物质的量浓度的各溶液 pH 关系为:pH(Na2CO3)>pH ( NaCN)>pH( CH3COONa)
B项:任何浓度下NaHCO3和 Na2CO3溶液的粒子种类必相同
C项:反应后相当于等浓度的NaCN与HCN的混合溶液,由于NaCN水解程度大于HCN的电离,故溶液为碱性,答案正确。
D项:c(Na+)="0.1" mol·L-1,由物料守恒知:c(CH3COO-)+c(CH3COOH)="0.2" mol·L-1;c(H+)=10—4 mol·L-1,很明确此项不正确
A项:越弱越水解,可知等物质的量浓度的各溶液 pH 关系为:pH(Na2CO3)>pH ( NaCN)>pH( CH3COONa)
B项:任何浓度下NaHCO3和 Na2CO3溶液的粒子种类必相同
C项:反应后相当于等浓度的NaCN与HCN的混合溶液,由于NaCN水解程度大于HCN的电离,故溶液为碱性,答案正确。
D项:c(Na+)="0.1" mol·L-1,由物料守恒知:c(CH3COO-)+c(CH3COOH)="0.2" mol·L-1;c(H+)=10—4 mol·L-1,很明确此项不正确

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
 H2CO3+2OH—
H2CO3+2OH—
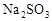


 比值增大
比值增大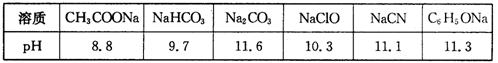



 。又知常温下某CuSO4溶液里
。又知常温下某CuSO4溶液里
 是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
 ,混合气体平均相对分子质量为 。
,混合气体平均相对分子质量为 。