题目内容
9.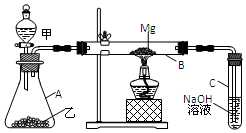 已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.用如图所示装置进行Mg和SO2反应的实验.
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性.用如图所示装置进行Mg和SO2反应的实验.(1)选择制取SO2的合适试剂②③.
①10%的H2SO4溶液 ②80%的H2SO4溶液
③Na2SO3固体 ④CaSO3固体
(2)写出装置乙和B中发生的主要反应的化学方程式:
Na2SO3+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+H2O+SO2↑;
3Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+MgS(或2Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+S,Mg+S$\frac{\underline{\;\;△\;\;}}{\;}$MgS).
装置C中NaOH溶液的作用是吸收过量二氧化硫,防止污染环境.
(3)你认为该装置是否有不足之处?有.如果有,请说明在A和B之间没有连接一个干燥装置、C装置未与大气相通、在镁下方未垫一个不锈钢片、镁与玻璃管反应、未设计一个防倒吸装置.
分析 (1)依据强酸制备弱酸的原理,结合物质的性质,选择实验室制备SO2的试剂;
(2)装置乙为制取SO2的反应;根据Mg与CO2的反应知B中Mg与SO2反应能生成氧化镁与单质硫,但单质硫能与镁反应生成硫化镁;二氧化硫有毒,不能直接排放到空气中,可用氢氧化钠吸收过量的二氧化硫;
(3)该装置中:①A中的水蒸气会进入B与Mg反应,在A、B中间应加干燥装置;②Mg能与SiO2反应,在Mg下方垫一不锈钢片,隔离Mg和SiO2;③尾气处理装置C试管用胶塞封闭,且无防倒吸装置.
解答 解:(1)依据强酸制备弱酸的原理,制取SO2应用浓H2SO4和亚硫酸盐,选项中不可选用CaSO3,因为CaSO3微溶于水,会附在固体表面,阻碍反应进行,
故答案为:②③;
(2)装置乙为制取SO2的反应,方程式为Na2SO3+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+H2O+SO2↑;Mg具有还原性,SO2具有氧化性,两者发生氧化还原反应,反应的方程式为3Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+MgS(或2Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+S,Mg+S$\frac{\underline{\;\;△\;\;}}{\;}$MgS),二氧化硫可与碱反应,易防止污染空气,所以装置C中NaOH溶液的作用是吸收过量二氧化硫,防止污染环境;
故答案为:Na2SO3+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO4+H2O+SO2↑;3Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+MgS(或2Mg+SO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+S,Mg+S$\frac{\underline{\;\;△\;\;}}{\;}$MgS);吸收过量二氧化硫,防止污染环境;
(3)该装置中:①A中的水蒸气会进入B与Mg反应,在A、B中间应加干燥装置;②Mg能与SiO2反应,在Mg下方垫一不锈钢片,隔离Mg和SiO2;③尾气处理装置C试管用胶塞封闭,且无防倒吸装置,
故答案为:有;在A和B之间没有连接一个干燥装置、C装置未与大气相通、在镁下方未垫一个不锈钢片、镁与玻璃管反应、未设计一个防倒吸装置.
点评 本题为信息题,以镁和二氧化硅的反应为载体考查了二氧化硫的实验室制备及性质检验,侧重培养学生分析问题解决问题的能力,题目难度较大.

 名校课堂系列答案
名校课堂系列答案| A. | 含有大量HCO3-的溶液中:NH4+、Na+、AlO2-、Cl- | |
| B. | PH=13的溶液中:Cl-、CO32-、K+、Na+ | |
| C. | 水电离c(OH-)=10-10mol/L的溶液中:NH4+、Na+、I-、Cl- | |
| D. | 能使甲基橙显红色的溶液中:Fe2+、K+、Cr2O72-、SO42- |
| A. | $C=\frac{1000m}{VM}$ | B. | $C=\frac{1000ρW}{M}$ | C. | $W%=\frac{CM}{1000ρ}$ | D. | $m=\frac{VρW}{1000}$ |
| A. | 温室效应--减少化石燃料使用,开发清洁能源 | |
| B. | 雾霾--适当限号,减少汽车尾气排放及扬尘 | |
| C. | 白色污染--杜绝生产塑料袋,从根源上治理 | |
| D. | 水体污染--节约用水,减少污水排放 |
| A. | KMnO4 | B. | H2O2 | C. | Cl2 水 | D. | HNO3 |
| 选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| A |  | AgNO3(aq) | AgOH(s) | Ag(NH3)2OH(aq) | NH3?H2O(aq) |
| B | S(s) | SO3(g) | SO2(g) | O2(g) | |
| C | NaOH(aq) | NaHCO3(aq) | Na2CO3(aq) | CO2(g) | |
| D | Fe(s) | Fe(NO3)2(aq) | Fe(NO3)3(aq) | HNO3(aq) |
| A. | A | B. | B | C. | C | D. | D |
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
| B | Mg(Al) | 过量稀盐酸 | 过滤 |
| C | FeCl2溶液(FeCl3) | 足量Fe粉 | 过滤 |
| D | CO2(CO) | O2 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
| A. | NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-5mol/L | |
| B. | Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序为:①=②>③ | |
| D. | 10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL |
