题目内容
3.16g KMnO4与50mL 12mol?L-1过量浓盐酸完全反应(假设浓盐酸无挥发),化学方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,通过计算回答:
(1)该反应中未被氧化的HCl的物质的量是 ;
(2)产生的Cl2在标准状况下的体积为多少升?
(3)在反应后的溶液中加足量的AgNO3溶液可生成多少克沉淀?
(1)该反应中未被氧化的HCl的物质的量是
(2)产生的Cl2在标准状况下的体积为多少升?
(3)在反应后的溶液中加足量的AgNO3溶液可生成多少克沉淀?
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:n( KMnO4)=
=0.02mol,n(HCl)=12mol/L×0.05L=0.6mol,
(1)根据方程式知,0.02mol高锰酸钾发生反应需要氯化氢的物质的量为0.32mol<0.6mol,所以盐酸有剩余,根据高锰酸钾和未被氧化的HCl之间的关系式计算;
(2)根据高锰酸钾和氯气之间的关系式计算氯气体积;
(3)根据氯原子守恒计算氯化银的质量.
| 3.16g |
| 158g/mol |
(1)根据方程式知,0.02mol高锰酸钾发生反应需要氯化氢的物质的量为0.32mol<0.6mol,所以盐酸有剩余,根据高锰酸钾和未被氧化的HCl之间的关系式计算;
(2)根据高锰酸钾和氯气之间的关系式计算氯气体积;
(3)根据氯原子守恒计算氯化银的质量.
解答:
解:n( KMnO4)=
=0.02mol,n(HCl)=12mol/L×0.05L=0.6mol,
(1)根据方程式知,0.02mol高锰酸钾发生反应需要氯化氢的物质的量为0.32mol<0.6mol,所以盐酸有剩余,该反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,如果有2mol高锰酸钾氧化,未被氧化的HCl的物质的量是6mol,则该反应中未被氧化的HCl的物质的量=
×6=0.06mol,
故答案为:0.06mol;
(2)高锰酸钾和氯气之间的关系式得氯气体积=
×5×22.4L/mol=1.12L,
答:产生的Cl2在标准状况下的体积为1.12L;
(3)根据高锰酸钾和被氧化的HCl的关系式知,被氧化的n(HCl)=
×10=0.1mol,根据氯原子守恒得溶液中n(Cl-)=0.6mol-0.1mol=0.5mol,根据氯原子守恒得n(Cl-)=n(AgCl)=0.5mol,则m(AgCl)=0.5mol×143.5g/mol=71.75g,答:在反应后的溶液中加足量的AgNO3溶液可生成71.75g沉淀.
| 3.16g |
| 158g/mol |
(1)根据方程式知,0.02mol高锰酸钾发生反应需要氯化氢的物质的量为0.32mol<0.6mol,所以盐酸有剩余,该反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,如果有2mol高锰酸钾氧化,未被氧化的HCl的物质的量是6mol,则该反应中未被氧化的HCl的物质的量=
| 0.02mol |
| 2 |
故答案为:0.06mol;
(2)高锰酸钾和氯气之间的关系式得氯气体积=
| 0.02mol |
| 2 |
答:产生的Cl2在标准状况下的体积为1.12L;
(3)根据高锰酸钾和被氧化的HCl的关系式知,被氧化的n(HCl)=
| 0.02mol |
| 2 |
点评:本题考查了氧化还原反应的有关计算,明确该反应中HCl的作用是解本题关键,再结合物质间的关系及原子守恒解答,题目难度中等.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
空气中的自由电子附着在分子或原子上形成的空气负离子(也叫阴离子)被称为“空气维生素”.O2-就是一种空气负离子,其摩尔质量为( )
| A、32 g |
| B、33 g |
| C、32 g?mol-1 |
| D、33 g?mol-1 |
下列物质的电子式书写正确的是( )
A、N2: |
B、CO2: |
C、Na2O: |
D、HCl: |
现有
X和
X+两种粒子,下列叙述正确的是( )
A Z |
A+1 Z |
| A、质子数相等 | ||
| B、X元素的质量数为A | ||
C、
| ||
| D、它们的化学性质几乎完全相同 |
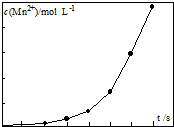 由软锰矿制备高锰酸钾的主要反应如下:
由软锰矿制备高锰酸钾的主要反应如下: