题目内容
反应H2(g)+I2(g)?2HI(g)在450℃时,化学平衡常数是49.则反应:HI(g)?
H2(g)+
I2(g) 在450℃时的化学平衡常数是( )
| 1 |
| 2 |
| 1 |
| 2 |
A、
| ||
B、
| ||
| C、7 | ||
D、
|
考点:化学平衡的计算
专题:化学平衡专题
分析:化学平衡常数指一定温度下可逆反应达到平衡,各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,故对于同一可逆反应,相同温度下,正、逆两个方向的平衡常数互为倒数,化学计量数为倍数关系时平衡常数为平方关系.
解答:
解:450℃时,反应H2(g)+I2(g)?2HI(g)的平衡常数为49,则2HI(g)?H2(g)+I2(g)的平衡常数K=
,则反应HI(g)?
H2(g)+
I2(g) 在450℃时的化学平衡常数是
=
=
,故选:A.
| 1 |
| 49 |
| 1 |
| 2 |
| 1 |
| 2 |
| K |
|
| 1 |
| 7 |
点评:本题考查平衡常数的书写、计算等,比较基础,掌握平衡常数的书写与意义即可解答.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目
氨的催化氧化4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-1025kJ?mol-1是工业制备硝酸的重要反应.一定条件下将4mol NH3和5mol O2混合并通入固定容积为2L的密闭容器中,经10s该反应达平衡,并测得NO的浓度为0.8mol?L-1.下列判断正确的是( )
| A、以O2浓度变化表示的反应速率为0.064 mol?(L?s)-1 | ||
| B、反应达到平衡状态时NH3的转化率为20% | ||
C、升高温度能使
| ||
| D、将容器的体积变为4 L,平衡时NO的浓度小于0.4 mol?L-1 |
下列操作不能达到实验目的或错误的是( )
A、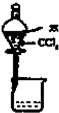 分离CCl4和水 |
B、 溶液的配制 |
C、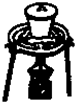 灼烧碳酸钙 |
D、 Na2CO3的焰色反应 |
在同温同压下,下列各组热化学方程式中 Q1<Q2的是(反应条件已略去)( )
| A、2H2(g)+O2(g)=2H2O(l);△H=-Q1,2H2(g)+O2(g)=2H2O (g);△H=-Q2 | ||||
| B、S(g)+O2(g)=SO2(g);△H=-Q1,S(s)+O2(g)=SO2(g);△H=-Q2 | ||||
C、C(s)+
| ||||
D、H2(g)+Cl2(g)=2HCl(g);△H=-Q1,
|