题目内容
20.有关杂化轨道的说法不正确的是( )| A. | 杂化前后的轨道数不变,但轨道的形状发生了改变 | |
| B. | sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180° | |
| C. | 部分四面体形、三角锥形、V形分子的结构可以用sp3杂化轨道解释 | |
| D. | 杂化轨道全部参加形成化学键 |
分析 A.原子轨道杂化前后轨道总数不变,但形状发生变化;
B.根据其空间构型判断夹角;
C.采用用sp3杂化的分子根据其含有的孤电子对个数确定其实际空间构型;
D.杂化轨道可以部分参加形成化学键.
解答 解:A.杂化前后的轨道数不变,杂化后,各个轨道尽可能分散、对称分布,导致轨道的形状发生了改变,故A正确;
B.sp3、sp2、sp杂化轨道其空间构型分别是正四面体、平面三角形、直线型,所以其夹角分别为109°28′、120°、180°,故B正确;
C.部分四面体形、三角锥形、V形分子的结构可以用sp3杂化轨道解释,如甲烷、氨气分子、水分子,故C正确;
D.杂化轨道可以部分参加形成化学键,例如NH3中N发生了sp3杂化,形成了4个sp3杂化杂化轨道,但是只有3个参与形成化学键,故D错误;
故选:D.
点评 本题考查了原子杂化,根据价层电子对互斥理论确定分子空间构型及原子杂化方式的判断,难度中等.

练习册系列答案
相关题目
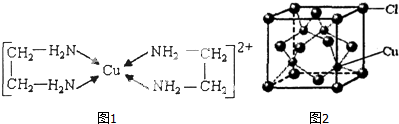
11.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为C<O<N.
(2)B的氢化物的分子空间构型是三角锥型.其中心原子采取sp3杂化.
(3)写出化合物AC2的电子式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
(4)ECl3与B、C的氢化物形成配位数为六的配合物的化学式为[Cr(NH3)4(H2O)2]Cl3.
| X | ||
| Y | ||
| Z |
(2)B的氢化物的分子空间构型是三角锥型.其中心原子采取sp3杂化.
(3)写出化合物AC2的电子式
 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.(4)ECl3与B、C的氢化物形成配位数为六的配合物的化学式为[Cr(NH3)4(H2O)2]Cl3.
15.以下仪器、用蒸馏水洗净后便可立即使用而不会对实验结果造成误差的是( )
①中和滴定用的锥形瓶;
②中和滴定用的滴定管;
③容量瓶;
④配制一定量、一定物质的量浓度的NaOH溶液,用于称量的小烧杯;
⑤量筒(中和热测定);
⑥移液管(量取醋酸).
①中和滴定用的锥形瓶;
②中和滴定用的滴定管;
③容量瓶;
④配制一定量、一定物质的量浓度的NaOH溶液,用于称量的小烧杯;
⑤量筒(中和热测定);
⑥移液管(量取醋酸).
| A. | ①②⑥ | B. | ①③ | C. | ①③⑤ | D. | ②④⑥ |
5.下列物质肯定为纯净物的是( )
| A. | 汽油 | B. | C2H6O | C. | 聚乙烯 | D. | 甘油 |
12.下列说法中错误的是( )
| A. | 只要是甜的物质,都是糖类 | |
| B. | 单糖是不能发生水解的最简单的糖类 | |
| C. | 淀粉纤维素都是天然有机高分子化合物 | |
| D. | 蔗糖和麦芽糖均为二糖 |
9.下列说法错误的是( )
| A. | 汽油是含有C5~C11的烷烃,可以通过石油的分馏得到汽油 | |
| B. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 | |
| C. | 取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等 | |
| D. | 煤含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来 |
3.甲醇是基本有机化工原料.甲醇及其可制得产品的沸点如下.
(1)在425℃、A12O3作催化剂,甲醇与氨气反应可以制得二甲胺.二甲胺显弱碱性,与盐酸反应生成(CH3)2NH2Cl,溶液中各离子浓度由大到小的顺序为c(Cl-)>c[(CH3)2NH2+]>c(H+)>c(OH-).
(2)甲醇合成二甲基甲酰胺的化学方程式为:2CH3OH+NH3+CO?(CH3)2NCHO+2H2O△H若该反应在常温下能自发进行,则△H<0 (填“>”、“<”或“=“).
(3)甲醇制甲醚的化学方程式为:2CH3OH?CH3OCH3+H2O△H.一定温度下,在三个体积均为1.0L 的恒容密闭容器中发生该反应.
①x/y=$\frac{1}{2}$.
②已知387℃时该反应的化学平衡常数K=4.若起始时向容器I中充入0.1mol CH3OH、
0,.15mol CH3OCH3和0.10mol H2O,则反应将向正(填“正”或“逆”)反应方向进行.
③容器Ⅱ中反应达到平衡后,若要进一步提高甲醚的产率,可以采取的措施为降温.
(4)以甲醇为主要原料,电化学合成碳酸二甲酯工作原理如图所示.
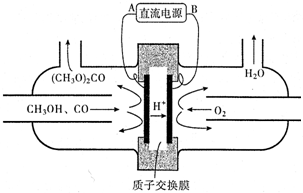
电源负极为B(填“A”或“B“),写出阳极的电极反应式2CH3OH+CO-2e-=(CH3O)2CO+2H+.
若参加反应的O2为1.12m3(标准状况),则制得碳酸二甲酯的质量为9.00kg.
| 名称 | 甲醇 | 二甲胺 | 二甲基甲酰胺 | 甲醚 | 碳酸二甲酯 |
| 结构式 | CH3OH | (CH3)2NH | (CH3)2NCHO | CH3OCH | (CH3O)2CO |
| 沸点(℃) | 64.7 | 7.4 | 153℃ | -24.9 | 90℃ |
(2)甲醇合成二甲基甲酰胺的化学方程式为:2CH3OH+NH3+CO?(CH3)2NCHO+2H2O△H若该反应在常温下能自发进行,则△H<0 (填“>”、“<”或“=“).
(3)甲醇制甲醚的化学方程式为:2CH3OH?CH3OCH3+H2O△H.一定温度下,在三个体积均为1.0L 的恒容密闭容器中发生该反应.
| 容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
| CH3OH | CH3OCH3 | H2O | ||
| Ⅰ | 387 | 0.20 | x | |
| Ⅱ | 387 | 0.40 | y | |
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
②已知387℃时该反应的化学平衡常数K=4.若起始时向容器I中充入0.1mol CH3OH、
0,.15mol CH3OCH3和0.10mol H2O,则反应将向正(填“正”或“逆”)反应方向进行.
③容器Ⅱ中反应达到平衡后,若要进一步提高甲醚的产率,可以采取的措施为降温.
(4)以甲醇为主要原料,电化学合成碳酸二甲酯工作原理如图所示.

电源负极为B(填“A”或“B“),写出阳极的电极反应式2CH3OH+CO-2e-=(CH3O)2CO+2H+.
若参加反应的O2为1.12m3(标准状况),则制得碳酸二甲酯的质量为9.00kg.
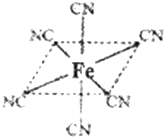 第四周期过渡元素Mn、Fe、Ti、Ni可与C、H、O形成多种化合物.
第四周期过渡元素Mn、Fe、Ti、Ni可与C、H、O形成多种化合物.