��Ŀ����
����Ŀ����13�֣�TiCl4�����Ѿ�����Ҫ�ɷ�ΪTiO2���Ʊ��ѣ�Ti������Ҫ�м����Ʊ���TiCl4������ʾ��ͼ���£�
���ϣ�TiCl4�����������Ȼ��������
������ | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
�е�/�� | 58 | 136 | 181�������� | 316 | 1412 |
�۵�/�� | -69 | -25 | 193 | 304 | 714 |
��TiCl4�е��ܽ��� | ���� | ���� | �� | ���� | |
��1���Ȼ����̣�TiO2��Cl2����ֱ�ӷ�Ӧ����̼����CO��CO2��ʹ��Ӧ���Խ��С�
��֪��TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ��H1=+175.4 kJ��mol-1
2C(s)+O2(g)=2CO(g) ��H2=-220.9 kJ��mol-1
�ٷ���¯�м�̼�Ȼ�����TiCl4(g)��CO(g)���Ȼ�ѧ����ʽ����
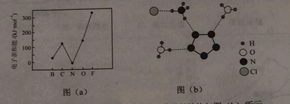
���Ȼ�������CO��CO2�����ת����������ͼ�жϣ�CO2����CO��Ӧ�Ħ�H0���������������=�������ж����ݣ���
���Ȼ���Ӧ��β���봦�����ŷţ�β���е�HCl��Cl2�����տɵô����ᡢFeCl3��Һ����β��������Һ��������
���Ȼ�������ȴ�����£������˵õ���TiCl4���Һ���������к�����
��2�����ƹ��̣���TiCl4����������ô�TiCl4��ʾ��ͼ���£�
����a�� �� T2Ӧ��������
���𰸡�
��1��TiO2(g)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ��H=-45.5kJ/mol�������¶�Խ�ߣ�CO�����ʵ���Խ���CO2�����ʵ���Խ�٣�˵��CO2����CO�ķ�Ӧ�����ȷ�Ӧ�����ԡ�H>0������ʳ��ˮ �Ȼ�������Һ��TiO2��C
��2�����Ȼ��裻136������
��������

����Ŀ�������£���ijBa��OH��2��Һ����μ���pH=x�����ᣬ��û����Һ�IJ���pH�����ʾ��
��� | ����������Һ�����/mL | ��������/mL | ��Һ��pH |
�� | 22.00 | 0.00 | 13 |
�� | 22.00 | 18.00 | 12 |
�� | 22.00 | 22.00 | 7 |
��1��Ba��OH��2��Һ�����ʵ���Ũ��Ϊ��
��2��x��ֵ�Ƕ��٣�
��3����100mL����Ba��OH��2��Һ����μ���0.05mol/L NaHCO3��Һ���������պô����ֵʱ��Һ��pHΪ���٣�����֪lg2=0.3��