题目内容
6.下列物质中只含有离子键的是( )| A. | H2 | B. | CO2 | C. | Na2O | D. | NaOH |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成共价键,第IA、第IIA族元素和第VIA、第VIIA族元素之间易形成离子键.
解答 解:A.氢气中只含非极性共价键,故A错误;
B.二氧化碳分子中碳原子和氧原子之间只存在共价键,为共价化合物,故B错误;
C.Na2O中钠离子和氧离子构成离子键,故C正确;
D.氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,故D错误;
故选C.
点评 本题考查了化学键的判断,难度不大,根据离子键、共价键的概念来分析解答即可,注意不能根据化合物的构成元素来确定化学键,为易错点.

练习册系列答案
相关题目
17.下列有关绿色化学的叙述中,不正确的是( )
| A. | 绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 | |
| B. | 最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物 | |
| C. | 绿色化学反应选择的原料、催化剂、溶剂都应该是无毒无害的 | |
| D. | 乙烯分别与溴水和溴的四氯化碳溶液反应制备1,2-二溴乙烷的原子利用率均为100% |
14.X、Y、Z、W为四种短周期主族元素,且原子序数依次递增,其中X、Z同族,Y是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,下列说法正确的是( )
| A. | Y、Z、W单核离子均能破坏水的电离平衡 | |
| B. | W元素氧化物对应水化物的酸性一定强于Z | |
| C. | 含X、Y、Z三种元素组成的化合物不止2种 | |
| D. | 因为X的氢化物分子间有氢键,所以X的氢化物较Z的氢化物稳定 |
11.我国在全球最先发现天然金属铀.下列对铀元素的一种核素的说法正确的是( )
| A. | 核电荷数为92 | B. | 质子数为143 | C. | 中子数为235 | D. | 核外电子数为235 |
18. 伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )
伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )
 伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )
伏打电堆(Voltaic pile)的照片和结构如图.它用圆形的锌板、铜板间隔堆积而成.所有的圆板之间夹放几层盐水泡过的布.下列说法正确的是( )| A. | 伏打电堆能将电能转化成化学能 | B. | 锌是正极 | ||
| C. | 盐水是电解质溶液 | D. | 伏打电堆工作时铜被还原 |
15.利用废旧铝合金(主要成分:Al、Fe、Mg)易拉罐制备钾明矾晶体[KAl(SO4)2•12H2O,式量474].制备步骤如下:
步骤1、铝片的准备
①去除易拉罐表面的漆膜;②用剪刀剪成小铝片,称2克备用
步骤2、钾明矾的制备
方案一:
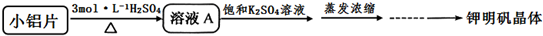
方案二:
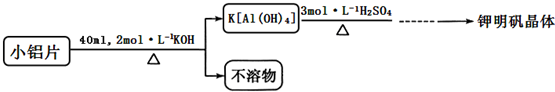
相关信息如下:
①钾明矾为正八面体晶型,有玻璃光泽,密度1.757g/cm3,熔点92.5℃.64.5℃时失去9分子结晶水,200℃时失去12分子结晶水,溶于水,难溶于乙醇.
②相关物质的溶解度:
请回答下列问题:
(1)下列方法不能去除易拉罐表面漆膜(主要成分为烃类化合物)的方法是B.
A.灼烧B.饱和碳酸钠溶液浸泡C.砂纸打磨D.有机溶剂浸泡
(2)方案一中的硫酸浓度不宜过稀也不宜过浓,原因是硫酸浓度过稀反应速率过慢,浓度过高会使铝片钝化;蒸发浓缩后的操作步骤是冷却结晶、过滤、洗涤、干燥;干燥时应控制温度64.5℃以下.
(3)实际实验中往往采用方案二,写出其可能的两条理由①方案一制备晶体中含有较多铁镁硫酸盐等杂质;②方案一反应速率较慢;方案二制备钾明矾晶体时为什么不再加入K2SO4饱和溶液?2K[Al(OH)4]+4H2SO4=K2SO4+Al2(SO4)3+8H2O(用方程式表示)
(4)最后得到钾明矾晶体质量为 31.5g,产率为89.7%.(保留3位有效数字)
步骤1、铝片的准备
①去除易拉罐表面的漆膜;②用剪刀剪成小铝片,称2克备用
步骤2、钾明矾的制备
方案一:
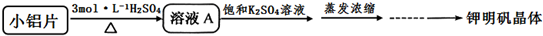
方案二:

相关信息如下:
①钾明矾为正八面体晶型,有玻璃光泽,密度1.757g/cm3,熔点92.5℃.64.5℃时失去9分子结晶水,200℃时失去12分子结晶水,溶于水,难溶于乙醇.
②相关物质的溶解度:
| 温度(℃) 物质 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| K2SO4 | 7.4 | 9.2 | 11.1 | 12.97 | 14.8 | 16.6 | 18.17 | 19.8 | 21.4 | 22.4 | 24.1 |
| Al2(SO4)3•18H2O | 31.2 | 33.5 | 36.4 | 40.4 | 45.7 | 52.2 | 59.2 | 66.2 | 73.1 | 86.8 | 89.0 |
| KAl(SO4)2•12H2O | 3.0 | 4.0 | 5.9 | 8.4 | 11.7 | 17.0 | 24.8 | 40.0 | 71.0 | 109.0 | 154.0 |
(1)下列方法不能去除易拉罐表面漆膜(主要成分为烃类化合物)的方法是B.
A.灼烧B.饱和碳酸钠溶液浸泡C.砂纸打磨D.有机溶剂浸泡
(2)方案一中的硫酸浓度不宜过稀也不宜过浓,原因是硫酸浓度过稀反应速率过慢,浓度过高会使铝片钝化;蒸发浓缩后的操作步骤是冷却结晶、过滤、洗涤、干燥;干燥时应控制温度64.5℃以下.
(3)实际实验中往往采用方案二,写出其可能的两条理由①方案一制备晶体中含有较多铁镁硫酸盐等杂质;②方案一反应速率较慢;方案二制备钾明矾晶体时为什么不再加入K2SO4饱和溶液?2K[Al(OH)4]+4H2SO4=K2SO4+Al2(SO4)3+8H2O(用方程式表示)
(4)最后得到钾明矾晶体质量为 31.5g,产率为89.7%.(保留3位有效数字)
 .
.