题目内容
17.已知H2(g)+Br2(l)=2HBr(g)△H=-72kJ•mol-1.蒸发1mol Br2(l)需要吸收的能量为30KJ,其他的相关数据如表:则表中a为( )| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 230 | a |
| A. | 369 | B. | 384 | C. | 469 | D. | 499 |
分析 焓变等于反应物中键能之和减去生成物中键能之和,以此来解答.
解答 解:蒸发1mol Br2(l)需要吸收的能量为30KJ,结合反应及表格中数据可知,436+(230+30)-2a=-72,解得a=384,
故选B.
点评 本题考查反应热与焓变,为高频考点,把握焓变与键能的关系、溴的状态为解答的关键,侧重分析与计算能力的考查,注意化学键数目的计算,题目难度不大.

练习册系列答案
相关题目
8.某化学反应的△H=-122kJ•mol-1,△S=+231J•mol-1•K-1,则此反应在下列哪种情况下可自发进行( )
| A. | 在任何温度下都能自发进行 | B. | 在任何温度下都不能自发进行 | ||
| C. | 仅在高温下自发进行 | D. | 仅在低温下自发进行 |
5.胶体区别于其它分散系的本质特征是( )
| A. | 胶体在一定条件下能稳定存在 | |
| B. | 光束通过胶体时有丁达尔效应 | |
| C. | 胶体粒子直径在1-100nm之间 | |
| D. | 胶体的分散质能通过滤纸空隙,而浊液的分散质不能 |
12.一包白色粉末,可能含有Na2CO3、CaCl2、NaI、CuSO4中的一种或几种,把它溶于水得无色澄清溶液,再加入用硝酸酸化的AgNO3溶液,有气体和沉淀产生,则原来的白色粉末( )
| A. | CaCl2,、Na2CO3 | B. | Na2CO3、NaI | ||
| C. | CaCl2、Na2CO3、NaI | D. | CaCl2、NaI |
2.四氟乙烯(CF2=CF2)是合成聚四氟乙烯(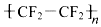 )的材料.
)的材料.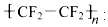 是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )
是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )
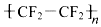 )的材料.
)的材料.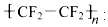 是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )
是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )| A. | CF2=CF2能使溴的CCl4溶液褪色 | |
| B. | 四氟乙烯合成聚四氟乙烯属于加聚反应 | |
| C. | 1molCF2=CF2只能与1molH2发生加成反应 | |
| D. | 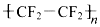 能使高锰酸钾酸性溶液褪色 能使高锰酸钾酸性溶液褪色 |
9.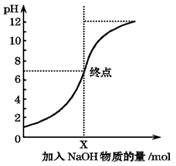 如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )
如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )
 如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )
如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )| A. | 原来盐酸的物质的量浓度为0.1mol/L | |
| B. | NaOH溶液的浓度为0.1mol/L | |
| C. | pH=1和pH=7的点对应溶液中水的电离程度相同 | |
| D. | X点NaOH溶液的体积为100mL |
6.下列实验操作正确的是( )
| A. | 将浓硫酸转移至容量瓶中,加水稀释至距标线2~3 cm处,改用胶头滴管定容 | |
| B. | 用酒精萃取碘水中的碘单质 | |
| C. | 进行液体蒸馏实验时,冷凝管中应充满自来水 | |
| D. | 某溶液加入盐酸酸化的氯化钡溶液后,出现白色沉淀,则原溶液中必有SO42- |
7.下列说法不正确的是( )
| A. | 运用蒸馏的方法,可以分离沸点相差较大的固体混合物 | |
| B. | 铁的化合物应用十分广泛,如FeCl3、FeSO4是优良的净水剂 | |
| C. | 镁燃烧发出耀眼的白光,常用于制造信号弹和焰火 | |
| D. | 工业上以氯气和石灰乳为原料制造漂白粉,漂白粉主要成分为Ca(ClO)2和CaCl2 |