题目内容
金属及其化合物转化关系是化学学习的重要内容之一.下列各组物质的转化关系中不全部是通过一步反应完成的是( )
| A、Na→NaOH→Na2CO3→NaCl |
| B、Fe→FeCl3→Fe(OH)3→Fe2O3 |
| C、Mg→MgCl2→Mg(OH)2→MgSO4 |
| D、Al→Al2O3→Al(OH)3→AlCl3 |
考点:常见金属元素的单质及其化合物的综合应用
专题:元素及其化合物
分析:A.钠与水反应生成NaOH,再与二氧化碳反应生成碳酸钠,最后与氯化钙反应生成氯化钠;
B.Fe与氯气反应生成氯化铁,再与NaOH反应生成沉淀,最后加热分解;
C.Mg与盐酸反应,再与NaOH反应,最后与硫酸反应;
D.Al2O3→Al(OH)3不能一步转化.
B.Fe与氯气反应生成氯化铁,再与NaOH反应生成沉淀,最后加热分解;
C.Mg与盐酸反应,再与NaOH反应,最后与硫酸反应;
D.Al2O3→Al(OH)3不能一步转化.
解答:
解:A.Na→NaOH→Na2CO3→NaCl中反应方程式分别为:2Na+2H2O=2NaOH+H2↑、2NaOH+CO2=Na2CO3 +H2O、Na2CO3+CaCl2=CaCO3↓+2NaCl,所以能一步实现,故A不选;
B.Fe→FeCl3→Fe(OH)3→Fe2O3 中反应方程式分别是2Fe+3Cl2
2FeCl3、FeCl3+3NaOH=Fe(OH)3↓+3NaCl、2Fe(OH)3
Fe2O3+3H2O,能一步实现,故B不选;
C.Mg→MgCl2→Mg(OH)2→MgSO4中反应方程式分别为:Mg+2HCl=MgCl2+H2↑、MgCl2+2NaOH=2NaCl+Mg(OH)2↓、Mg(OH)2+H2SO4=MgSO4+2H2O,能一步实现,故C不选;
D.氧化铝和水不反应,所以不能一步生成氢氧化铝,故D选;
故选D.
B.Fe→FeCl3→Fe(OH)3→Fe2O3 中反应方程式分别是2Fe+3Cl2
| ||
| ||
C.Mg→MgCl2→Mg(OH)2→MgSO4中反应方程式分别为:Mg+2HCl=MgCl2+H2↑、MgCl2+2NaOH=2NaCl+Mg(OH)2↓、Mg(OH)2+H2SO4=MgSO4+2H2O,能一步实现,故C不选;
D.氧化铝和水不反应,所以不能一步生成氢氧化铝,故D选;
故选D.
点评:本题考查金属及化合物转化及性质,为高频考点,明确物质的性质是解本题关键,注意把握Na、Mg、Al、Fe为知识点构建知识网络,归纳元素化合物知识,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
浓硫酸具有强烈的吸水性、脱水性与强的氧化性等多重特性,在中学化学实验中经常用浓硫酸制取气体,在以下实验使用的硫酸采用较高浓度的原因不是基于上述特性的是( )
| A、实验室利用Na2SO3与硫酸制取SO2气体时,一般采用浓度较大的硫酸 |
| B、向白纸上滴几滴浓硫酸 |
| C、向浓硫酸中滴加浓盐酸制取HCl气体 |
| D、利用金属Cu与浓硫酸反应制取SO2气体 |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A、含氧酸的酸性:X对应的酸性强于Y对应的酸性 |
| B、第一电离能Y不一定小于X |
| C、X与Y形成化合物时,X显负价,Y显正价 |
| D、Y的气态氢化物的稳定性小于X气态氢化物的稳定性 |
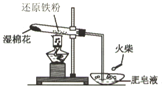 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验.
为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验.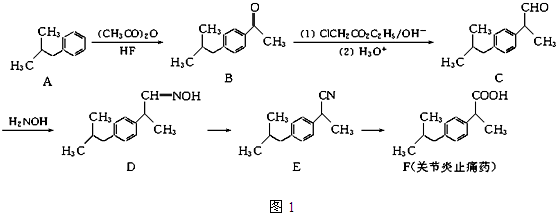


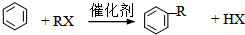
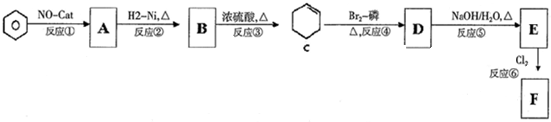
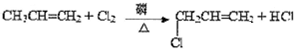 F的结构简式为
F的结构简式为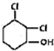
 直接制
直接制 ,理由是
,理由是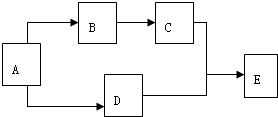 有A、B、C、D、E五种物质,在一定条件下的相互转化关系如图所示.已知:常温下E为无色液体,C、D为无色气体单质,A为金属单质,B为淡黄色固体,请回答下列问题:
有A、B、C、D、E五种物质,在一定条件下的相互转化关系如图所示.已知:常温下E为无色液体,C、D为无色气体单质,A为金属单质,B为淡黄色固体,请回答下列问题: