题目内容
(10分)实验室要配制480 mL 0.2 mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有__________________(填选项的字母)。
A.烧杯 B.500 mL容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为_______________g。
(3)取用任意体积的该NaOH溶液时,下列物理量中不随所取体积的多少而变化的是_______。
A.溶液中NaOH的物质的量 B.溶液的浓度
C.溶液中OH-的数目 D.溶液的密度
(4)在配制上述溶液的过程中,下列情况对 NaOH溶液物质的量浓度有何影响(填“偏高”、“偏低”、或“无影响”)
①未经冷却趁热将溶液注入容量瓶中:______________
②容量瓶用蒸馏洗涤后残留有少量的水:_____________
③定容时某同学观察液面的情况如图所示,则所配制的溶液的浓度____________。
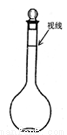
④转移溶液后,未洗涤烧杯和玻璃棒就直接定容___________。(“偏低”、或“无影响”)
(10分)(1)C (2分)
(2)4.0(2分)
(3)BD(2分)
(4)①偏高(1分)
②无影响(1分) ③偏高(1分) ④偏低(1分)
【解析】
试题分析:(1)配制溶液时,需要烧杯溶解固体,用玻璃棒进行搅拌,容量瓶盛放溶液,胶头滴管定容,所以不用漏斗,答案选C;
(2)配制480 mL 0.2 mol/L NaOH溶液,应选择500mL的容量瓶,所以需要称量氢氧化钠的质量是0.5L×0.2mol/L×40g/mol=4.0g;
(3)氢氧化钠的物质的量和氢氧根离子的数目都与溶液的体积有关,而溶液的浓度与密度是溶液固有的属性,不随溶液的体积变化而变化,所以答案选BD;
(4)①氢氧化钠溶于水放热,未经冷却直接将溶液移入容量瓶,则会使溶液的体积偏小,氢氧化钠溶液的浓度偏高;
②在配制的过程中,需直接滴加蒸馏水,所以容量瓶内有少量的蒸馏水对实验的结果无影响;
③定容时俯视刻度线,使所配溶液的体积偏小,溶液的浓度偏高;
④未洗涤烧杯、玻璃棒,会使溶质的物质的量减少,所配溶液的物质的量浓度偏低。
考点:考查溶液的配制与计算

 阅读快车系列答案
阅读快车系列答案(12分)有一化学反应2A  B+D ,B、D起始浓度为0,在四种不同条件下进行。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表,根据下述数据,完成填空:
B+D ,B、D起始浓度为0,在四种不同条件下进行。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表,根据下述数据,完成填空:
实验 序号 | 浓度(mol/L) | 时间(min) | |||||||
0 | 10 | 20 | 30 | 40 | 50 | 60 | |||
1 | 温度 | 800 ℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800 ℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 | |
3 | 800 ℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 | |
(1)在实验1,反应在0至40分钟时间内A的平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度C2= mol/L,可推测实验2中隐含的条件是
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则达到平衡时v3 v1(填>、=、<=,)800℃时,反应平衡常数= ,且C3= mol/L,可推测实验3中隐含的条件是 。
(4)800℃时,反应B+D  2A当其他条件不变, B、D的起始浓度为0.50 mol/L , A的起始浓度为0,达到平衡时A的浓度为 mol/L, B的转化率= 。
2A当其他条件不变, B、D的起始浓度为0.50 mol/L , A的起始浓度为0,达到平衡时A的浓度为 mol/L, B的转化率= 。
 B.
B.
 D.
D.