题目内容
经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.下列判断正确的是( )
分析:Al的电负性为1.5,K的电负性为0.8,Mg的电负性为1.2,Si的电负性为1.8,P的电负性为2.1,Cl的电负性为3.0,以此可判断电负性差值,并判断化合物类型,如不清楚电负性的具体值,可根据活泼金属与活泼非金属形成的化合物为离子化合物,非金属元素形成的化合物为共价化合物,以此判断.
解答:解:A.Al的电负性为1.5,Cl的电负性为3.0,电负性差值为1.5,小于1.7,为共价键,则AlCl3为共价化合物,故A错误;
B.Si的电负性为1.8,Cl的电负性为3.0,电负性差值为1.2,小于1.7,为共价键,SiCl4为共价化合物,故B正确;
C.P的电负性为2.1,Cl的电负性为3.0,电负性差值为0.9,小于1.7,为共价键,故C错误;
D.K与Mg都是金属,二者之间不能形成共价键,况且电负性差值为0.4,故D错误.
故选B.
B.Si的电负性为1.8,Cl的电负性为3.0,电负性差值为1.2,小于1.7,为共价键,SiCl4为共价化合物,故B正确;
C.P的电负性为2.1,Cl的电负性为3.0,电负性差值为0.9,小于1.7,为共价键,故C错误;
D.K与Mg都是金属,二者之间不能形成共价键,况且电负性差值为0.4,故D错误.
故选B.
点评:本题考查电负性与共价键、离子键的关系,题目难度不大,注意元素周期表中电负性的递变规律.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
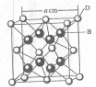 (2011?咸阳模拟)[化学-选修物质结构与性质]
(2011?咸阳模拟)[化学-选修物质结构与性质]