题目内容
【题目】如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( ) 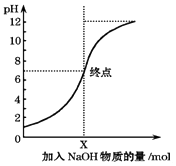
A.原来盐酸的物质的量浓度为0.1mol/L
B.NaOH溶液的浓度为0.1mol/L
C.pH=1和pH=7的点对应溶液中水的电离程度相同
D.X点NaOH溶液的体积为100mL
【答案】A
【解析】解:A.由图可知,盐酸的pH=1,则盐酸的物质的量浓度为0.1mol/L,故A正确;
B.n(HCl)=n(NaOH),可知n(NaOH)=0.1L×0.1mol/L=0.01mol,体积未知,不能计算浓度,故B错误;
C.盐酸抑制水的电离,而pH=7时溶质为NaCl,对水的电离无影响,对水的电离无影响,故C错误;
D.NaOH的浓度未知,不能计算其体积,故D错误;
故选A.

 名校课堂系列答案
名校课堂系列答案【题目】用0.1032molL﹣1 HCl溶液滴定未知浓度的NaOH溶液,
(1)某同学按下列步骤进行实验:①取一锥形瓶,用待测NaOH溶液润洗两次; ②在锥形瓶中加入 25,.00 mL待测NaOH溶液;③加入几滴石蕊试剂做指示剂;④取一支酸式滴定管,洗涤干净; ⑤直接往酸式滴定管中注入标准酸溶液,进行滴定; ⑥两眼注视着滴定管内盐酸溶液液面下降,直至滴定终点.
其中所述操作有错误的序号为
(2)取用25.00 mL待测NaOH溶液应用以下(选填:“甲”、“乙”)装置,若取用NaOH溶液开始平视读数、结束时俯视读数,会导致所测氢氧化钠溶液浓度(填“偏大““偏小“或“不变“) ![]()
(3)若滴定开始前滴定管尖嘴中有一气泡,滴定结束后气泡消失, 则会导致所测氢氧化钠溶液浓度(填“偏大““偏小“或“不变“)
(4)若平行实验三次,记录的数据如下表
滴定次数 | 待测溶液的体积(/mL) | 标准HCl溶液的体积 | |
滴定前读数(/mL) | 滴定后读数(/mL) | ||
① | 25.00 | 1.02 | 21.04 |
② | 25.00 | 2.00 | 22.98 |
③ | 25.00 | 0.20 | 20.18 |
试计算待测NaOH溶液的物质的量浓度(列出计算过程).