题目内容
图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列反应对应的曲线错误的是( )

| A、D是向含有等物质的量的Ca (OH)2、KOH的混合溶液中通入CO2至沉淀消失 |
| B、C是向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量 |
| C、B是向澄清石灰水中通入CO2至过量 |
| D、A是向NaAlO2溶液中滴入HCl至过量 |
考点:化学方程式的有关计算,镁、铝的重要化合物
专题:图示题
分析:A、根据反应2OH-+CO2═CO32-+H2O,Ca2++CO32-═CaCO3↓,CO32-+CO2+H2O═2HCO3-,CaCO3+CO2+H2O═Ca(HCO3)2判断.
B、根据反应Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O 判断;
C、根据反应Ca(OH)2+CO2═CaCO3↓+H2O,CaCO3+CO2+H2O═Ca(HCO3)2判断;
D、根据反应AlO2-+H++H2O═Al(OH)3↓,Al(OH)3+3H+═Al3++3H2O判断;
B、根据反应Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O 判断;
C、根据反应Ca(OH)2+CO2═CaCO3↓+H2O,CaCO3+CO2+H2O═Ca(HCO3)2判断;
D、根据反应AlO2-+H++H2O═Al(OH)3↓,Al(OH)3+3H+═Al3++3H2O判断;
解答:
解:A、向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至沉淀消失,发生的反应分别为2OH-+CO2═CO32-+H2O,Ca2++CO32-═CaCO3↓,CO32-+CO2+H2O═2HCO3-,CaCO3+CO2+H2O═Ca(HCO3)2,设Ca(OH)2的物质的量为xmol,则各段反应消耗的二氧化碳的物质的量分别为x,1.5x,x比值为2:3:2,故A错误;
B、向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量,发生的反应分别为OH-+H+═H20,Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,后两个反应消耗的NaOH的物质的量之比为3:1,图象符合,故B正确;
C、向澄清石灰水中通入CO2至过量,发生的反应分别为Ca(OH)2+CO2═CaCO3↓+H2O,CaCO3+CO2+H2O═Ca(HCO3)2,两个反应消耗的二氧化碳的物质的量之比为1;1,图象符合,故C正确;
D、向NaAlO2溶液中滴入HCl至过量,发生的反应分别为AlO2-+H++H2O═Al(OH)3↓,Al(OH)3+3H+═Al3++3H2O,两个反应消耗的盐酸的物质的量之比为1:3,图象符合,故D正确.
故选:A.
B、向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量,发生的反应分别为OH-+H+═H20,Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,后两个反应消耗的NaOH的物质的量之比为3:1,图象符合,故B正确;
C、向澄清石灰水中通入CO2至过量,发生的反应分别为Ca(OH)2+CO2═CaCO3↓+H2O,CaCO3+CO2+H2O═Ca(HCO3)2,两个反应消耗的二氧化碳的物质的量之比为1;1,图象符合,故C正确;
D、向NaAlO2溶液中滴入HCl至过量,发生的反应分别为AlO2-+H++H2O═Al(OH)3↓,Al(OH)3+3H+═Al3++3H2O,两个反应消耗的盐酸的物质的量之比为1:3,图象符合,故D正确.
故选:A.
点评:本题考查物质反应的图象题,题目难度中等,注意每个反应的各组分反应的量的关系.

练习册系列答案
相关题目
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大.X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其原子的电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )
| A、Z与Y形成的化合物可作为耐高温材料 |
| B、WY2能与碱反应,但不能与任何酸反应 |
| C、原子半径按X、Y、Z、R、W的顺序依次增大 |
| D、熔沸点:X2R>X2Y |
 有两个密闭容器A和B,容器A有一个可以移动的活塞,能使容器内保持恒压,容器B保持恒容,起始时向容器A和B中分别充入等物质的量的SO3气体,并使两容器的容积相等(如图所示).在保持400℃的条件下发生反应:2SO3(g)?2SO2(g)+O2(g).则下列描述正确的是( )
有两个密闭容器A和B,容器A有一个可以移动的活塞,能使容器内保持恒压,容器B保持恒容,起始时向容器A和B中分别充入等物质的量的SO3气体,并使两容器的容积相等(如图所示).在保持400℃的条件下发生反应:2SO3(g)?2SO2(g)+O2(g).则下列描述正确的是( )| A、达到平衡所需要的时间:A容器更短 |
| B、达到平衡时:B容器中SO3的转化率更大 |
| C、达到平衡时:A容器中SO2的物质的量更多 |
| D、达到平衡时:A容器中SO3的体积分数更大 |

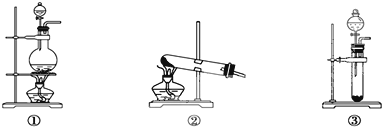
 泡沫灭火器的原理,在小试管中装入硫酸铝溶液,吸滤瓶中装入碳酸氢钠溶液,原理分析:发生水解相互促进的反应:Al2(SO4)3+6NaHCO3═3Na2SO4+2Al(OH)3↓+6CO2↑.
泡沫灭火器的原理,在小试管中装入硫酸铝溶液,吸滤瓶中装入碳酸氢钠溶液,原理分析:发生水解相互促进的反应:Al2(SO4)3+6NaHCO3═3Na2SO4+2Al(OH)3↓+6CO2↑.