题目内容
 如图所示,A、B、C、D、G是五种常见单质,其中A、G为气体.化合物R在常温下呈液态,F为黑色晶体,H为淡黄色粉末,I是玻璃工业的一种原料,图中部分生成物已略去.试回答下列问题:
如图所示,A、B、C、D、G是五种常见单质,其中A、G为气体.化合物R在常温下呈液态,F为黑色晶体,H为淡黄色粉末,I是玻璃工业的一种原料,图中部分生成物已略去.试回答下列问题:(1)H的电子式:


(2)写出化学反应方程式:
反应①
3Fe+4H2O
Fe3O4+4H2
| ||
3Fe+4H2O
Fe3O4+4H2
;
| ||
反应③
Na2CO3+Al2O3
2NaAlO2+CO2↑
| ||
Na2CO3+Al2O3
2NaAlO2+CO2↑
;
| ||
(3)C与T溶液反应的离子方程式:
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
;(4)5.4gC在G中燃烧放出166.9kJ热量,反应②的热化学方程式为:
4Al(S)+3O2(g)=2Al2O3(S)△H=-3338kJ/mol
4Al(S)+3O2(g)=2Al2O3(S)△H=-3338kJ/mol
.分析:“A、G为气态单质”,且能相互化合生成R(液态),则R为H2O;A、G、分别为H2和O2中的一种,再结合“G+B(单质)→H(淡黄色粉末)”可推知A、B、G、H依次为H2、Na、O2、Na2O2;T为NaOH.
“D(单质)分别与G(O2)、R(H2O)反应,都可生成F(黑色晶体)”,可知D为金属单质且为Fe,F为Fe3O4.
“C(单质)+G(O2)→M,且M可以与T(NaOH反应)”则M必为酸性或两性氧化物.再结合F(Fe3O4)与C生成M(C的氧化物)的反应可知该反应为铝热反应,故可推知C、M、N依次为Al、
Al2O3、NaAlO2.
“I为玻璃工业的(三种)原料之一”,且可以分别由H(Na2O2)、T(NaOH)得到,则I为Na2CO3,E为CO2.
结合物质的性质解答该题.
“D(单质)分别与G(O2)、R(H2O)反应,都可生成F(黑色晶体)”,可知D为金属单质且为Fe,F为Fe3O4.
“C(单质)+G(O2)→M,且M可以与T(NaOH反应)”则M必为酸性或两性氧化物.再结合F(Fe3O4)与C生成M(C的氧化物)的反应可知该反应为铝热反应,故可推知C、M、N依次为Al、
Al2O3、NaAlO2.
“I为玻璃工业的(三种)原料之一”,且可以分别由H(Na2O2)、T(NaOH)得到,则I为Na2CO3,E为CO2.
结合物质的性质解答该题.
解答:解:“A、G为气态单质”,且能相互化合生成R(液态),则R为H2O;A、G、分别为H2和O2中的一种,再结合“G+B(单质)→H(淡黄色粉末)”可推知A、B、G、H依次为H2、Na、O2、
Na2O2;T为NaOH.
“D(单质)分别与G(O2)、R(H2O)反应,都可生成F(黑色晶体)”,可知D为金属单质且为Fe,F为Fe3O4.
“C(单质)+G(O2)→M,且M可以与T(NaOH反应)”则M必为酸性或两性氧化物.再结合F(Fe3O4)与C生成M(C的氧化物)的反应可知该反应为铝热反应,故可推知C、M、N依次为Al、
Al2O3、NaAlO2.
“I为玻璃工业的(三种)原料之一”,且可以分别由H(Na2O2)、T(NaOH)得到,则I为Na2CO3,E为CO2.
(1)H为Na2O2,为离子化合物,电子式为 ,故答案为:
,故答案为: ;
;
(2)①F为Fe3O4,R为H2O,D为为Fe,该反应为Fe和水的反应,化学方程式为,3Fe+4H2O
Fe3O4+4H2,故答案为:3Fe+4H2O
Fe3O4+4H2;
②反应③为Na2CO3和Al2O3的反应,生成NaAlO2,反应的化学方程式为Na2CO3+Al2O3
2NaAlO2+CO2↑,故答案为:Na2CO3+Al2O3
2NaAlO2+CO2↑;
(3)C为Al,能与NaOH溶液反应生成NaAlO2和H2,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)C为Al,G为O2,Al与O2反应生成Al2O3,反应的化学方程式为4Al+3O2
2Al2O3,当n(Al)=
=0.2mol时,放出166.9kJ热量,则4molAl反应放出3338kJ的热量,反应②的热化学方程式为4Al(S)+3O2(g)=2Al2O3(S)△H=-3338kJ/mol,
故答案为:4Al(S)+3O2(g)=2Al2O3(S)△H=-3338kJ/mol.
Na2O2;T为NaOH.
“D(单质)分别与G(O2)、R(H2O)反应,都可生成F(黑色晶体)”,可知D为金属单质且为Fe,F为Fe3O4.
“C(单质)+G(O2)→M,且M可以与T(NaOH反应)”则M必为酸性或两性氧化物.再结合F(Fe3O4)与C生成M(C的氧化物)的反应可知该反应为铝热反应,故可推知C、M、N依次为Al、
Al2O3、NaAlO2.
“I为玻璃工业的(三种)原料之一”,且可以分别由H(Na2O2)、T(NaOH)得到,则I为Na2CO3,E为CO2.
(1)H为Na2O2,为离子化合物,电子式为
 ,故答案为:
,故答案为: ;
;(2)①F为Fe3O4,R为H2O,D为为Fe,该反应为Fe和水的反应,化学方程式为,3Fe+4H2O
| ||
| ||
②反应③为Na2CO3和Al2O3的反应,生成NaAlO2,反应的化学方程式为Na2CO3+Al2O3
| ||
| ||
(3)C为Al,能与NaOH溶液反应生成NaAlO2和H2,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)C为Al,G为O2,Al与O2反应生成Al2O3,反应的化学方程式为4Al+3O2
| ||
| 5.4g |
| 27g/mol |
故答案为:4Al(S)+3O2(g)=2Al2O3(S)△H=-3338kJ/mol.
点评:本题考查无机物的推断,题目难度较大,答题时注意题中所给各物质的性质,根据反应的关系可采用正、逆推相结合的方法推断.

练习册系列答案
相关题目


 如图所示,a、b、c、d均为石墨电极,通电一段时间后,各电极上的生成物的物质的量之比依次为4:1:2:2,则甲、乙两池中的电解质分别是( )
如图所示,a、b、c、d均为石墨电极,通电一段时间后,各电极上的生成物的物质的量之比依次为4:1:2:2,则甲、乙两池中的电解质分别是( )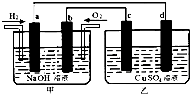 如图所示,a、b、c、d为惰性电极.甲装置中a、b两个电极上分别通入H2、O2,电解质溶液为NaOH溶液,乙装置中电解质溶液为CuSO4溶液,下列有关说法正确的是( )
如图所示,a、b、c、d为惰性电极.甲装置中a、b两个电极上分别通入H2、O2,电解质溶液为NaOH溶液,乙装置中电解质溶液为CuSO4溶液,下列有关说法正确的是( ) 在10L密闭容器中,某放热反应进行过程在不同反应时间各物质的量的变化情况如图所示(A、B、C均为气体),则:
在10L密闭容器中,某放热反应进行过程在不同反应时间各物质的量的变化情况如图所示(A、B、C均为气体),则: