题目内容
1.NA代表阿伏加德罗常数的值,下列说法正确的是( )| A. | 5.6 g 铁在足量氯气中燃烧,电子转移0.2 NA个 | |
| B. | 7.8 g的Na2O2与足量的水反应后溶液的体积为1L,该溶液的物质的量浓度为0.2mol/L | |
| C. | 1.12 L氯气中含有0.1 NA个氯原子 | |
| D. | 标准状况下,2.24 LSO3中含有0.3NA个氧原子 |
分析 A.铁与氯气反应后铁元素变为+3价;
B.过氧化钠与水反应生成氢氧化钠,2Na2O2+2H2O=O2↑+4NaOH,结合C=$\frac{n}{V}$解答;
C.气体状况未知;
D.标况下,三氧化硫不是气体.
解答 解:A.氯气的氧化性很强,铁与氯气反应后铁元素变为+3价,故5.6g铁即0.1mol铁反应时转移0.3mol电子,故A错误;
B.7.8 g的Na2O2与足量的水反应生成0.2mol氢氧化钠,溶液体积为1L,则氢氧化钠溶液物质的量浓度C=$\frac{0.2mol}{1L}$=0.2mol/L,故B正确;
C.气体状况未知,无法计算氯气的物质的量和氯原子个数,故C错误;
D.标况下,三氧化硫不是气体,不能使用气体摩尔体积,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的相关计算,掌握公式的使用和物质的结构是解题关键,注意气体摩尔体积使用条件和对象,题目难度中等.

练习册系列答案
相关题目
9.五种短周期元素在元素周期表中的位置如图所示,其中X元素最高正化合价与最低负化合价的代数和为0,下列判断正确的是( )
| X | |||||
| Z | Y | M | N |
| A. | 原子半径:Y>X | |
| B. | 阴离子还原性:N>M | |
| C. | 最高价氧化物对应水化物的碱性:Y>Z | |
| D. | 气态氢化物稳定性:M>N |
10.在Na+浓度为0.9mol•L-1的某澄清溶液中,还可能含有下表中的若干种离子:
取该溶液100ml进行如下实验(气体体积在标准状况下测定):
I.向该溶液中加入足量稀HCl,产生白色沉淀并放出1.12L气体
II.将I的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称得固体质量为3.6g
III.在II的滤液中滴加BaCl2溶液,无明显现象
下列说法不正确的是( )
| 阳离子 | K+、Ag+、Mg2+、Ba2+ |
| 阴离子 | NO3-、CO32-、SiO32-、SO42- |
I.向该溶液中加入足量稀HCl,产生白色沉淀并放出1.12L气体
II.将I的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称得固体质量为3.6g
III.在II的滤液中滴加BaCl2溶液,无明显现象
下列说法不正确的是( )
| A. | K+一定存在,且c(K+)≤1.3mol•L-1 | |
| B. | 实验I能确定一定不存在的离子是Ag+、Mg2+、Ba2+ | |
| C. | 实验I中生成沉淀的离子方程式为SiO32-+2H+=H2SiO3↓ | |
| D. | 实验III能确定一定不存在SO42- |
6.钓鱼岛群岛的东海海域及部分太平洋海域探明为海底热水矿床.海底热水矿床是沉积着由岩浆热气从地底喷出的金、铜、锌、稀有金属等区域.下列说法正确的是( )
| A. | 金不溶于任何溶液 | |
| B. | 铜、锌在空气中均能被氧化成对应的氧化物 | |
| C. | 铜锌合金的熔点低于铜或锌的熔点 | |
| D. | ${\;}_{29}^{63}$Cu的质子数和中子数之差为34 |
13.制备下列气体过程中,净化除杂的有关操作(括号内是杂质),正确的是( )
| A. | CO2(CO):气体通过灼热的CuO | |
| B. | Cl2(SO2):通入盛有品红溶液的洗气瓶 | |
| C. | NO(NO2):通过水洗,再干燥后,用向下排空气法收集 | |
| D. | H2(CO2):依次通过盛有氢氧化钠溶液和浓硫酸的洗气瓶 |
10.下列物质中,属于电解质的是( )
| A. | Fe | B. | H2SO4 | C. | CH4 | D. | 酒精 |
11.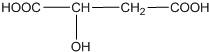 近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )
 近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )| A. | 苹果酸在一定条件下能发生酯化反应 | |
| B. | 苹果酸在一定条件下能发生催化氧化反应 | |
| C. | 苹果酸在一定条件下能发生消去反应 | |
| D. | 1mol苹果酸与金属钠作用,最多能产生3mol氢气 |
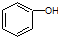 和
和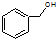
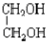 与
与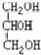

 .
.