题目内容
2A(g)?2B(g)+C(g)△H<0,现欲使正反应速率减小,C的浓度增大,可行的措施是( )
| A、加压 | B、增大C的浓度 |
| C、减少C的浓度 | D、降温 |
考点:化学平衡的影响因素
专题:
分析:对反应2A(g)?2B(g)+C(g)△H<0,减小B和C的浓度反应速率下降,但C的浓度减小,而减小压强,平衡正向移动,C的浓度增大,使用负催化剂正反应速率减小,但平衡不移动,C的浓度不变,而正反应是放热反应去分析解答.
解答:
解:A、加压,正反应速率加快,故A错误;
B、增大C的浓度,正反应速率加快,故B错误;
C、减少C的浓度,正反应速率减小,但C的浓度变小,故C错误;
D、正反应是放热反应,降温正反应速率减小,平衡正向移动,C的浓度变大,故D正确;
故选:D.
B、增大C的浓度,正反应速率加快,故B错误;
C、减少C的浓度,正反应速率减小,但C的浓度变小,故C错误;
D、正反应是放热反应,降温正反应速率减小,平衡正向移动,C的浓度变大,故D正确;
故选:D.
点评:本题考查化学反应速率、化学平衡影响因素、难度中等,注意基础知识理解掌握,注意掌握外界条件对反应速率的影响.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
下列实验操作中叙述正确的是( )
| A、萃取操作必须在分液漏斗中进行 |
| B、用酒精灯直接加热蒸馏烧瓶 |
| C、用剩的药品应收集起来放回原试剂瓶中 |
| D、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 |
分子中具有手性碳原子的是 ( )
| A、甘油 |
| B、3-甲基己烷 |
| C、2-甲基-1-丁烯 |
| D、2,2-二甲基丙烷 |
下列燃料中,不属于化石燃料的是( )
| A、煤 | B、石油 | C、天然气 | D、水煤气 |
下列物质不会造成大气污染的是( )
| A、二氧化硫 | B、氮气 |
| C、一氧化碳 | D、氮氧化物 |
菜在生长的过程中,常喷洒农药防治虫害.据有关专家介绍,用碱性溶液或清水浸泡,
可使残留在蔬菜上的农药的毒性降低.因此,买来的蔬菜在食用之前最好用稀碱水或清水浸泡一段时间,浸泡蔬菜时可加入适量( )
可使残留在蔬菜上的农药的毒性降低.因此,买来的蔬菜在食用之前最好用稀碱水或清水浸泡一段时间,浸泡蔬菜时可加入适量( )
| A、纯碱 | B、白酒 | C、白糖 | D、食醋 |
下列离子方程式书写正确的是( )
| A、向明矾溶液加入过量氨水:Al3++4OH-═〔Al(OH)4〕- |
| B、碳酸钙溶于稀盐酸:CO32-+2H+═H2O+CO2↑ |
| C、SO2通入足量的Ba(NO3)2稀溶液中:3SO2+2H2O+2NO3-+3Ba2+═3BaSO4↓+2NO+4H+ |
| D、一小块钠投入到CuSO4溶液中:2Na+Cu2+═Cu+2Na+ |
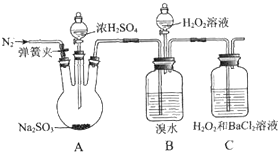 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).
为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验).