题目内容
3.溶质的物质的量浓度相同的 HCl(aq)、H2SO4(aq)、CH3COOH(aq)各100mL,①水的电离程度最大的是醋酸溶液②分别与同样的锌粒反应,开始时反应速率最快的是硫酸溶液(写名称).
分析 ①酸或碱抑制水电离,酸中氢离子或碱中氢氧根离子浓度越大,其抑制水电离程度越大;
②物质的量浓度相同的 HCl(aq)、H2SO4(aq)、CH3COOH(aq)分别与同样的锌反应,反应速率与氢离子浓度成正比.
解答 解:①酸或碱抑制水电离,酸中氢离子或碱中氢氧根离子浓度越大,其抑制水电离程度越大,醋酸是弱电解质导致部分电离,硫酸是二元强酸,物质的量浓度相同的盐酸、硫酸和醋酸,氢离子浓度大小顺序是:硫酸、盐酸、醋酸,则抑制水电离程度大小顺序是:硫酸、盐酸、醋酸,所以水电离程度最大的是醋酸,
故答案为:醋酸;
②物质的量浓度相同的 HCl(aq)、H2SO4(aq)、CH3COOH(aq)分别与同样的锌反应,反应速率与氢离子浓度成正比,物质的量浓度相同的这三种酸中,氢离子浓度大小顺序是硫酸、盐酸、醋酸,则反应速率最大的是硫酸,故答案为:硫酸.
点评 本题考查水电离影响因素、反应速率影响因素等知识点,为高频考点,化学反应速率与离子浓度成正比、与电荷成正比,与电解质强弱无关,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.依据反应原理:NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl,并利用下列装置制取碳酸氢钠粗品,实验装置正确且能达到实验目的是( )
| A. |  用装置制取氨气 | B. |  用装置制取二氧化碳 | ||
| C. |  用装置制取碳酸氢钠 | D. |  用装置分离碳酸氢钠与母液 |
18.常温时,以下4种溶液pH最小的是( )
| A. | 0.02mol/L醋酸溶液与等体积的水混合 | |
| B. | 0.02mol/L醋酸与0.02mol/LNaOH溶液等体积混合液 | |
| C. | 0.03mol/L醋酸与0.01mol/LNaOH溶液等体积混合液 | |
| D. | pH=2的盐酸与pH=12的NaOH溶液等体积混合液 |
8.下面关于电解质的叙述中错误的是( )
| A. | 在水溶液里或熔融状态下能够导电的化合物叫做电解质 | |
| B. | 电解质、非电解质都指化合物而言,单质不属于此范畴 | |
| C. | NH3的水溶液可以导电,所以NH3是电解质 | |
| D. | 纯水的导电性虽然很差,但是水是电解质 |
15.下列不能用勒夏特列原理解释的是( )
| A. | Fe(SCN)3溶液中加入固体KSCN后颜色变深 | |
| B. | 棕红色NO2加压后颜色先变深后变浅 | |
| C. | 打开碳酸型饮料的瓶盖,有大量的气体从饮料中冒出 | |
| D. | 用高压锅蒸煮食物更省时间 |
12.有关电解质的说法正确的是( )
| A. | 强电解质的水溶液导电性要比弱电解质的水溶液导电性强 | |
| B. | SO2水溶液的导电性很好,所以 SO2是电解质 | |
| C. | 液态的铜导电性很好,所以铜是电解质 | |
| D. | 强电解质的水溶液中不存在溶质分子 |
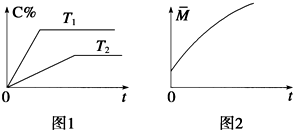 在密闭容器中投入一定量的A和B发生反应:
在密闭容器中投入一定量的A和B发生反应: