题目内容
16.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 28g${\;}_{6}^{14}$C中含有的质子数为14NA | |
| B. | 1mol苯乙酸中所含碳碳双键数为4NA | |
| C. | 1L 2mol/L的NaClO水溶液中含有的氧原子数为2NA | |
| D. | 标准状况下,3.36L NO2和足量水充分反应转移的电子数为0.1NA |
分析 A.结合n=$\frac{m}{M}$及质子数为6计算;
B.苯乙酸中不含碳碳双键;
C.水中含O原子;
D.n(NO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,发生3NO2+H2O=2HNO3+NO,该反应转移2e-,以此来解答.
解答 解:A.n=$\frac{m}{M}$=$\frac{28g}{14g/mol}$=2mol,含质子数为2mol×6×NA=12NA,故A错误;
B.苯乙酸中不含碳碳双键,则不能计算碳碳双键数目,故B错误;
C.水中含O原子,则溶液中含有的氧原子数远大于2NA,故C错误;
D.n(NO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,发生3NO2+H2O=2HNO3+NO,该反应转移2e-,则和足量水充分反应转移的电子数为0.15mol×$\frac{1}{3}$×(4-2)×NA=0.1NA,故D正确;
故选D.
点评 本题考查物质的量计算及阿伏伽德罗常数,为高频考点,把握物质的量的相关计算公式、物质的组成、氧化还原反应等为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
4.某有机物结构简式为: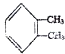 ,按系统命名法命名,下列命名正确的是(
,按系统命名法命名,下列命名正确的是(
 ,按系统命名法命名,下列命名正确的是(
,按系统命名法命名,下列命名正确的是(| A. | 对二甲苯 | B. | 1,6-二甲苯 | C. | 1,2-二甲苯 | D. | 乙苯 |
11.取H2和CO的混合气体6g,与6.4g氧气恰好完全反应,将其产物与足量过氧化钠固体完全反应,反应后固体的质量增加多少 ( )
| A. | 6.4g | B. | 6g | C. | 12.4g | D. | 8.8g |
1.25℃时氯水含Cl2、HClO和ClO-组份φ%(以物质的量计算)分布图如下,下列结论正确的是( )

| A. | n(Cl2)、n(HClO)和n(ClO-)之和不随pH变化而变化 | |
| B. | 当pH逐渐增大时,HClO先增大后减小 | |
| C. | 当pH>8.5时,c(H+)=c(OH-)+c(ClO-)+c(Cl-) | |
| D. | K1、K2均是通过曲线交点计算得出的酸的电离平衡常数 |
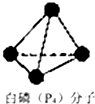 氨是重要的化工原料,用途广泛.
氨是重要的化工原料,用途广泛.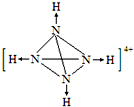 .
. 已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):
已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去): ;D
;D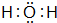 .
.