题目内容
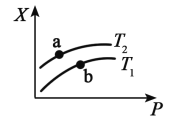
【题目】在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是![]()
A.在含![]() 、
、![]() 、
、![]() 的溶液中逐滴加入硫酸氢钠溶液:
的溶液中逐滴加入硫酸氢钠溶液:![]() 、
、![]() 、
、![]()
B.含等物质的量的![]() 、
、![]() 的溶液中,缓慢通入氯气:
的溶液中,缓慢通入氯气:![]() 、
、![]() 、
、![]()
C.含等物质的量的![]() 、KOH的溶液中,缓慢通入
、KOH的溶液中,缓慢通入![]() :KOH、
:KOH、![]() 、
、![]() 、
、![]()
D.在含![]() 、
、![]() 、
、![]() 的溶液中逐渐加入烧碱溶液:
的溶液中逐渐加入烧碱溶液:![]() 、
、![]() 、
、![]()
【答案】A
【解析】
A.硫酸氢钠溶液显酸性,加入硫酸氢钠后先发生中和反应,结合氢离子的能力OH->AlO2->SO32-,与氢离子反应的先后顺序为:OH-、AlO2-、SO32-,故A正确;
B.离子还原性I->Fe2+>Br-,氯气先与还原性强的反应,还原性强弱顺序是I-、Fe2+、Br-,因为2Fe2++Br2=2Fe3++2Br-,故B错误;
C.在含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2,先和氢氧根反应生成碳酸根,钡离子结合碳酸根生成碳酸钡沉淀,所以最先反应的是氢氧化钡,其次是氢氧化钾,继续通入二氧化碳,溶液中的碳酸钾与二氧化碳、水反应生成碳酸氢钾,最后碳酸钡沉淀溶解生成碳酸氢钡,则反应先后顺序为:Ba(OH)2、KOH、K2CO3、BaCO3,故C错误;
D.在含等物质的量的Fe3+、H+、NH4+的溶液中,逐滴加入NaOH溶液,先后反应顺序和与氢氧根结合能力有关,结合后的物质越难电离,则结合能力越强,先反应,水为极弱的电解质,所以先和H+反应,铁盐与氨水反应生成氢氧化铁沉淀,所以铁离子先和氢氧根反应,所以反应先后顺序为:H+、Fe3+、NH4+,故D错误。
故选A。

【题目】新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高电子层符号为__,该电子层具有的原子轨道数为__。
②LiBH4由Li+和BH4-构成,BH4-的立体构型是__,B原子的杂化轨道类型是___。
③Li、B元素的电负性由小到大的顺序为___。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+__H-(填“>”“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是__族元素。
(3)图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和涂“![]() ”分别标明B与N的相对位置___。
”分别标明B与N的相对位置___。
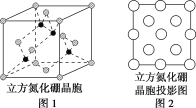
(4)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,H-的半径为__,NaH的理论密度是__g·cm-3(保留3个有效数字)。