题目内容
16.现有常温条件下甲、乙、丙三种溶液,甲为0.1mol•L-1的NaOH溶液,乙为0.1mol•L-1的盐酸,丙为未知浓度的FeCl2溶液,试回答下列问题:(1)甲溶液的pH=13.
(2)丙溶液中存在的化学平衡有Fe2++2H2O?Fe(OH)2+2H+、H2O?OH-+H+(用离子方程式表示).
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为丙>甲=乙.
分析 (1)0.1mol•L-1的NaOH溶液中c(OH-)=0.1mol/L,根据Kw=c(H+)•c(OH-)计算溶液中c(H+),再根据pH=-logc(H+)计算溶液的pH值;
(2)溶液中存在亚铁离子的水解平衡和水的电离平衡;
(3)酸或碱抑制水电离,含有弱根离子的盐促进水电离.
解答 解:(1)0.1mol•L-1的NaOH溶液中c(OH-)=0.1mol/L,故溶液中c(H+)=$\frac{1{0}^{-14}}{0.1}$mol/L=10-13mol/L,故该溶液的pH=-log10-13=13,
故答案为:13;
(2)溶液中存在亚铁离子的水解平衡和水的电离平衡离子方程式为Fe2++2H2O?Fe(OH)2+2H+、H2O?OH-+H+;
故答案为:Fe2++2H2O?Fe(OH)2+2H+、H2O?OH-+H+;
(3)酸或碱抑制水电离,含有弱根离子的盐促进水电离,乙酸是弱电解质,氢氧化钠、氯化氢是强电解质,所以相同物质的量浓度的乙酸和盐酸和氢氧化钠,盐酸中水电离出的氢氧根离子浓度小于醋酸,相同物质的量浓度的盐酸和氢氧化钠对水电离抑制程度相等,盐酸中水电离出的氢氧根离子浓度等于氢氧化钠溶液中水的电离,所以水电离出氢氧根离子浓度大小顺序是:丙>甲=乙,
故答案为:丙>甲=乙.
点评 本题综合考查酸碱混合的定性判断和计算以及弱电解质的电离和盐类的水解等知识,题目难度中等.答题时注意审题.注意掌握溶液酸碱性与溶液pH的关系结合图象进行判断是解答本题关键.

练习册系列答案
相关题目
7.下列说法正确的是( )
| A. | 为了提取电子垃圾中有用的金属,可将其进行焚烧 | |
| B. | 模型一般可分为物体模型和思维模型 | |
| C. | 某同学研究SO2性质的程序是分类(预测SO2的化学性质)→观察(得出SO2的物理性质)→实验→比较并得出结论 | |
| D. | 科学实验能解决化学学科的所有问题 |
11. 25℃时,电离平衡常数:
25℃时,电离平衡常数:
回答下列问题:
(l)物质的量浓度均为0.1mol•L-l的下列四种溶液:
a.Na2CO3溶液;b.NaClO溶液;c.CH3COONa溶液;d.NaHCO3溶液.
pH由大到小的顺序是A>B>D>C(填编号).
(2)常温下0.1mol•L-l的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(3)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如下图则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数;理由是pH相同的醋酸和HX稀释相同的倍数,HX的pH变化大稀释后,HX溶液中水电离出来的c(H+)大于 醋酸溶液中水电离出来的c(H+)无用填“大于”、“等于”或“小于”)理由是稀释后醋酸中氢离子浓度大于HX,所以醋酸抑制水电离程度大于HX.
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol/L(填准确数值).
 25℃时,电离平衡常数:
25℃时,电离平衡常数:| 化学试 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K14.3×10-7 K25.6×10-11 | 3.0×10-8 |
(l)物质的量浓度均为0.1mol•L-l的下列四种溶液:
a.Na2CO3溶液;b.NaClO溶液;c.CH3COONa溶液;d.NaHCO3溶液.
pH由大到小的顺序是A>B>D>C(填编号).
(2)常温下0.1mol•L-l的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(3)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如下图则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数;理由是pH相同的醋酸和HX稀释相同的倍数,HX的pH变化大稀释后,HX溶液中水电离出来的c(H+)大于 醋酸溶液中水电离出来的c(H+)无用填“大于”、“等于”或“小于”)理由是稀释后醋酸中氢离子浓度大于HX,所以醋酸抑制水电离程度大于HX.
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol/L(填准确数值).
8. T℃时,将一定量的混合气体在密闭容器中发生反应aA(g)+bB(g)?cC(g)+dD(g),平衡后测得B气体的浓度为0.6mol/L,恒温下,将密闭容器中的容积扩大1倍,重新达到平衡后,测得B气体的浓度为0.4mol/L,下列叙述正确的是( )
T℃时,将一定量的混合气体在密闭容器中发生反应aA(g)+bB(g)?cC(g)+dD(g),平衡后测得B气体的浓度为0.6mol/L,恒温下,将密闭容器中的容积扩大1倍,重新达到平衡后,测得B气体的浓度为0.4mol/L,下列叙述正确的是( )
 T℃时,将一定量的混合气体在密闭容器中发生反应aA(g)+bB(g)?cC(g)+dD(g),平衡后测得B气体的浓度为0.6mol/L,恒温下,将密闭容器中的容积扩大1倍,重新达到平衡后,测得B气体的浓度为0.4mol/L,下列叙述正确的是( )
T℃时,将一定量的混合气体在密闭容器中发生反应aA(g)+bB(g)?cC(g)+dD(g),平衡后测得B气体的浓度为0.6mol/L,恒温下,将密闭容器中的容积扩大1倍,重新达到平衡后,测得B气体的浓度为0.4mol/L,下列叙述正确的是( )| A. | 重新达到平衡时,D的体积分数减小 | B. | a+b<c+d | ||
| C. | 平衡向右移动 | D. | 重新达到平衡时,A气体浓度增大 |
5.银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag2O、Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn+H2O═2Ag+Zn(OH)2.下列说法中错误的是( )
| A. | 原电池放电时,负极上发生反应的物质是Zn | |
| B. | 负极上发生的反应是Zn+2OH--2e-═Zn(OH)2 | |
| C. | 工作时,负极区溶液pH减小,正极区pH增大 | |
| D. | 溶液中OH-向正极移动,K+、H+向负极移动 |
6.能正确表示下列化学反应的离子方程式的是( )
| A. | 氢氧化钡溶液与稀硫酸的反应 OH-+H+═H2O | |
| B. | 氧化钙与稀盐酸反应 CaO+2H+═Ca2++H2O | |
| C. | 铁片插入硝酸银溶液中 Fe+Ag+═Fe2++Ag | |
| D. | 碳酸钙溶于稀硝酸中 CO32-+2H+═CO2↑+H2O |
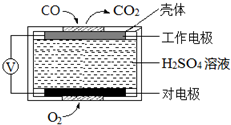 碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题.
碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题.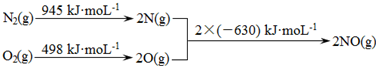
 某温度时,在VL密闭容器中,A、B、C三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析:
某温度时,在VL密闭容器中,A、B、C三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析: