题目内容
【题目】某密闭容器中发生如下反应:X(g)+3Y(g) ![]() 2Z(g);ΔH<0下图表示该反应的速率(v)随时间(t)变化的关系,t2,t3,t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
2Z(g);ΔH<0下图表示该反应的速率(v)随时间(t)变化的关系,t2,t3,t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
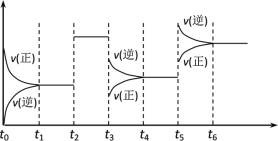
A.t2升高温度B.t3时降低了温度
C.t5时增大了压强D.t5~t6时间内转化率最低
【答案】D
【解析】
由图可知,t2时正逆反应速率同等程度增大;t3时正逆反应速率均减小,但逆反应速率大,平衡逆向移动;t5时正逆反应速率均增大,且平衡逆向移动,结合可逆反应的特点及平衡移动来解答。
A. 该反应为正反应放热的反应,t2若为升高温度,则平衡逆向移动,图像中t2时正逆反应速率同等程度增大,应为使用催化剂,故A错误;
B. 该反应为放热反应,且气体体积减小的反应,t3时正逆反应速率均减小,但逆反应速率大,平衡逆向移动,则应为减小压强,故B错误;
C. 该反应为放热反应,且气体体积减小的反应,t5时正逆反应速率均增大,且平衡逆向移动,则应为升高温度,故C错误;
D. 由图可知,t5~t6段,t5时平衡逆向移动,则t6时反应物的转化率比前面所有时刻都低,故D正确;
答案选D。

练习册系列答案
相关题目
【题目】几种短周期元素的原子半径及主要化合价如下表:下列叙述正确的是( )
元素代号 | X | Y | Z | W |
原子半径/pm | 160 | 143 | 70 | 66 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
A.X、W元素的离子半径 W<X
B.一定条件下,W单质可以与Z元素的氢化物发生化学反应
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,Z单质与W的常见单质直接生成ZW2