题目内容
12.对于核电荷数为37的元素,有如下各项的描述,其中正确的是( )| A. | 该元素的单质在常温下跟水反应不如钠剧烈 | |
| B. | 该元素的原子半径比钾的原子半径小 | |
| C. | 该元素的碳酸盐难溶于水 | |
| D. | 该元素最高价氧化物的水化物能使Al(OH)3溶解 |
分析 依据原子核外电子排布规律可知核电荷数为37的元素核外有4个电子层,各层容纳电子数分别为2、8、18、8、1,为第五周期第ⅠA族元素,依据同主族元素性质的递变规律结合钠、钾的性质解答.
解答 解:依据原子核外电子排布规律可知核电荷数为37的元素核外有4个电子层,各层容纳电子数分别为2、8、18、8、1,为Rb,为第五周期第ⅠA族元素,
A.Rb排在钠、钾的下面,与钠、钾同主族,金属性强于钠,钾,常温下跟水反应比钠剧烈,故A错误;
B.Rb电子层数多于钾,原子半径大于钾,故B错误;
C.依据碳酸钠、碳酸钾易溶于水可知碳酸銣易溶于水,故C错误;
D.Rb排在钠、钾的下面,金属性强于钠和钾,对应最高价氧化物的水化物碱性强于氢氧化钠和氢氧化钾,能够与氢氧化铝反应生成可溶性偏铝酸銣,故D正确.
故选D.
点评 本题考查了碱金属的性质,为高频考点,侧重于元素化合物以及元素周期率的考查,熟悉同主族元素性质的递变规律是解题关键,题目难度不大.

练习册系列答案
相关题目
3.如图是一个能对负载供电的电池装置.下列说法正确的是( )
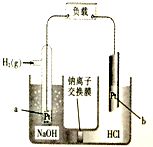

| A. | b极是负极 | |
| B. | a极电极反应式为H2-2e-═2H+ | |
| C. | 负载通过1mol电子,右池产生标况下5.6L气体 | |
| D. | 电池总反应式为:H++OH-═H2O |
20.实验室用溴和苯反应制取溴苯.得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④10%NaOH溶液洗.正确的操作顺序是( )
| A. | ①②③④② | B. | ②④①②③ | C. | ④②③①② | D. | ②④②③① |
17.某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取Cl2,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4 $\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+2Cl2↑+2H2O,他们设计了如下实验用于制取Cl2并验证其某些性质.
请回答:
(1)该实验中A部分的装置是②(填写装置的序号).

(2)若要证明B中Na2SO3溶液已被氧化,所需要的化学试剂为BaCl2溶液、稀盐酸;
(3)实验进行了一段时间后,他们要探究C中FeSO4溶液被氧化的程度,设计了以下的方案,请填写其中的空白:
(4)完成酸性KMnO4溶液滴入FeSO4溶液中的离子反应方程式:
1Mn${O}_{4}^{-}$+5Fe2++8H+=1Mn2++5Fe3++4H2O.

请回答:
(1)该实验中A部分的装置是②(填写装置的序号).

(2)若要证明B中Na2SO3溶液已被氧化,所需要的化学试剂为BaCl2溶液、稀盐酸;
(3)实验进行了一段时间后,他们要探究C中FeSO4溶液被氧化的程度,设计了以下的方案,请填写其中的空白:
| 实验目的 | 操作与结论 |
| ①FeSO4溶液完全未被氧化 | 实验①取少许溶液于试管中,滴入数滴KSCN溶液,若溶液不变色(选填“不变色”或“变红色”),说明溶液完全未被氧化. |
| ②FeSO4部分被氧化 | ②实验②:取少许溶液于试管中,滴入数滴酸性KMnO4溶液,若溶液褪色;再另取少许溶液于试管中,滴加几滴KSCN溶液,溶液变 红(血红)色,说明溶液被部分氧化. |
| ③FeSO4完全被氧化 | ③重复实验②在待测②液中滴加数滴酸性KMnO4溶液后,溶液不褪色,另一实验现象与②同. |
1Mn${O}_{4}^{-}$+5Fe2++8H+=1Mn2++5Fe3++4H2O.
1.下列分子式表示的物质一定是纯净物的是( )
| A. | C5H10 | B. | CH4 | C. | C2H4O2 | D. | C2H4Cl2 |
2.下列生活或生产中的事实不能用化学反应速率的有关原理解释的是( )
| A. | 有些药物的标签上注明必须冷藏 | |
| B. | 铵态氮肥与草木灰不能同时施用 | |
| C. | 在接触室中加入五氧化二钒使二氧化硫与氧气在其表面反应 | |
| D. | 劈碎的木材燃烧更旺 |

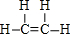 ;B的结构简式:CH3CH3;
;B的结构简式:CH3CH3;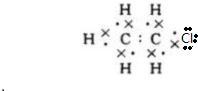 ;D的官能团名称羟基;G官能团的结构简式-COOH.
;D的官能团名称羟基;G官能团的结构简式-COOH.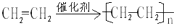 (反应类型加聚反应).
(反应类型加聚反应).


